Послеоперационные кровотечения в кардиохирургии
Патологическое кровотечение – это отделение крови по дренажам, которое выходит за рамки «нормальной» кровопотери после кардиотомии. Это частое осложнение операций на сердце. Редко оно является острым и жизнеугрожающим, поскольку кровопотеря может возмещаться с адекватной скоростью. Тем не менее, оно должно лечиться агрессивно, поскольку само кровотечение усугубляет коагулопатию и увеличивает общую заболеваемость.
«Нормальная» кровопотеря
Кровопотеря по дренажам средостения в норме максимальна в течение первых часов после операции и снижается практически до нуля в течение последующих 6-12 часов. Приемлемый объём кровопотери в различных больницах варьирует, что зависит от большого числа периоперационных факторов. Тем не менее, приемлемая скорость кровопотери примерно одинакова: до 2 мл/кг*час в течение первых 2-3 часов, до 1 мл/кг*час в течение последующих 3 часов и менее 0,5 мл/кг*час к 12 часу после операции. При этом скорость кровопотери должна уменьшаться.
Тампонада сердца
Тампонада сердца – это жизнеугрожающее состояние, требующее неотложной помощи. Оно является показанием к экстренной рестернотомии (см. Рестернотомия по поводу кровотечения). Тампонада не всегда легко диагностируется.
Тампонаду следует подозревать при:
- Гипотензии, при которой давление зависит от акта дыхания
- Уменьшении диуреза и нарастании ацидоза, несмотря на введение диуретиков
- Выравнивании давлений наполнения правого и левого желудочков
- Внезапном прекращении поступления крови по дренажам
- Выраженном расширении средостения на рентгенограмме грудной клетки
- Снижении вольтажа на ЭКГ
- Тахикардии и аритмиях, в том числе при ФЖ и ЭМД
Эхоскопия средостения может указать на наличие сгустка в перикарде, сдавление ПЖ и ЛЖ в диастолу.
NB! Гипотензия, повышение давлений наполнения и тахиаритмии на фоне кровотечения могут также быть связаны с сердечной недостаточностью, напряжённым пневмотораксом и массивной ТЭЛА. Эти клинические признаки не являются показанием к рестернотомии, которая может быть фатальной при этих состояниях.
Этиология
Дооперационные факторы
Приём некоторых препаратов: аспирина, клопидогреля, варфарина, тромболитиков, абциксимаба, коагулопатия, возраст, стернотомии в анамнезе, инфекционный эндокардит. Дооперационный выпот в плевральной полости может имитировать кровотечение, если эта полость не дренирована.
Операционные факторы
Хирургические манипуляции, ИК вызывает нарушение функций тромбоцитов, тромбоцитопению и активирует фибринолиз; остаточный гепарин.
Послеоперационные факторы
Гемодилюция, массивная трансфузионная терапия эрмассой, гипотермия, гипертензия, несовершенные («старые») дренажи и излишне подвижный пациент.
Лечение
Предотвратите периоперационную кровопотерю: определите и корригируйте имеющуюся у пациента коагулопатию. Некоторые анестезиологи профилактически вводят апротинин и транексамовую кислоту (см. Препараты крови и прокоагулянты). Вероятнее всего, самым важным фактором является тщательная хирургическая техника.
Обследование
- Взгляните на пациента и быстро ответьте на вопросы: пациент гемодинамически нестабилен? кровь поступает по дренажам очень быстро? кровь на вид артериальная? отмечается ли кровоточивость мест забора шунтов и мест установки катетеров?
- Массивное кровотечение часто требует эмпирического лечения, ещё до получения результатов исследования системы свёртывания: возмещайте массивную кровопотерю препаратами крови.
- Узнайте результат АВСК после нейтрализации гепарина.
- Если рана при ушивании выглядела влажной, наберите кровь для определения фибринолиза, АЧТВ, ПТВ, ТВ и уровня фибриногена сразу при поступлении в ОИТР, а также выполняйте этот анализ после каждой партии препаратов крови при лечении кровотечения.
- Если, несмотря на проведенную коррекцию АЧТВ, ПТВ и числа тромбоцитов, кровотечение продолжается, проверьте уровень свободного гепарина и D-димеров.
- Рентгенограмма грудной клетки может указать на гемоторакс или выраженное расширение средостения. Выполните также эхоскопическое исследование плевральных полостей, перикарда.
- При подозрении на серозно-геморрагический характер отделяемого по дренажу (что может наблюдаться при наличии у пациента плеврального выпота до операции, промывании грудной клетки в конце операции) определите уровень Hb в дренажной жидкости.
- Тромбоэластограмма используется редко, однако она полезна в качестве экспресс-диагностики нарушений свёртывания.
Лечение массивного кровотечения
Если скорость кровотечение достигает 500 мл за 30 минут или пациент гемодинамически нестабилен, приготовьтесь к экстренной рестернотомии (см. Рестернотомия по поводу кровотечения).
Определите параметры свёртывающей системы крови, гемоглобин. При необходимости закажите 2-3 дозы эрмассы, СЗП и концентрат тромбоцитов. Рассмотрите необходимость использования аппарата «Cell-Saver».
Для поддержания среднего АД при анемии проведите трансфузию эрмассы, ГЭК или гелофузина, если эрмасса недоступна или не показана. При гипотензии опустите головной конец кровати вниз.
Введите 25 мг протамина: если он хорошо переносился в операционной, то будет хорошо переноситься и в ОИТР. Помните: введение протамина оправдано при выявлении свободного гепарина в тесте на АВСК с гепариназой.
Избегайте введения большого объёма холодных растворов: применяйте грелки для растворов. Избегайте также введения большого объёма коллоидных объёмзамещающих растворов; их применение оправдано при гиповолемии и недоступности препаратов крови.
Согрейте пациента до 37°C:гипотермия подавляет механизмы свёртывания крови и функцию тромбоцитов.
Контролируйте гипертензию с помощью адекватной седации и вазодилятации, купируйте дрожь с помощью седации и миорелаксации (см. Типичные гемодинамические синдромы).
Увеличьте РЕЕР: это может уменьшить кровопотерю за счёт «тампонирования» венозных источников кровотечения в грудной клетке, но также снижает наполнение сердца, вызывая гипотензию.
По показаниям вводите тромбоциты, СЗП, эрмассу, протамин или криопреципитат (см. Препараты крови и прокоагулянты).Рассмотрите необходимость введения апротинина (0,5 миллиона единиц в час в течение 6 часов) или транексамовой кислоты. Следует помнить, что некоторые анестезиологи избегают введения обоих препаратов, поскольку сообщалось о риске острого тромбоза шунтов.
Отсрочьте приём аспирина и других антикоагулянтов. При кровотечениирегулярно проверяйте состояние дренажей, чтобы гарантировать их проходимость, регулярно их «сдаивайте».При окклюзии дренажа отсоедините его и быстро удалите сгусток пинцетом.Может понадобиться аспирация сгустков из дренажа с помощью стерильного аспирационного катетера небольшого диаметра, подсоединённого к вакууму.

Источник
Несмотря на то, что послеоперационные кровотечения у кардиохирургических больных являются частыми и грозными осложнениями, в вопросе о профилактике и лечении этого осложнения еще многое остается спорным и нерешенным. В настоящей работе анализируются случаи кровотечения у 74 больных, что составляет 4,1% на 1791 оперированного больного по поводу сердечно-сосудистой патологии в период с 1999 по 2004 г.
Во внимание принималась кровопотеря 20% и более общего объема крови больного. У 80% больных это осложнение развилось в первые часы и сутки после операции.
Частота кровотечения в зависимости от диагноза и условий выполнения хирургического вмешательства представлена в таблице.
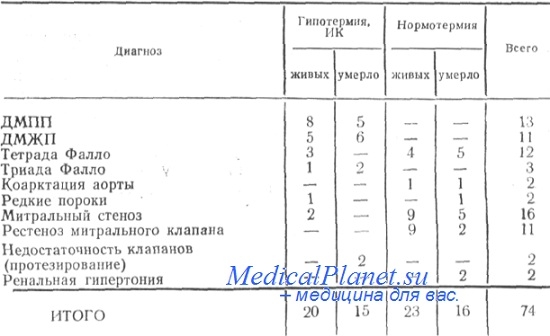
Как видно из таблицы, высокая частота кровотечений имела место у больных, оперированных в условиях «открытого» сердца—35, у больных, оперированных по поводу рестеноза митрального клапана— 11.
Летальный исход, вызванный кровотечением, был у 31 больного (1,7%), что на 175 умерших за этот период равно 17,2%. Следует подчеркнуть, что из 31 умершего больного кровотечение, как причина смерти при патоморфологическом исследовании, установлено лишь у 17. У остальных 14 умерших, где кровотечение, как причина смерти, не вызвала сомнений, летальность по заключению патоморфологов наступила от сердечно-сосудистой слабости — 10, иочечпо-печеиочной недостаточности— 4.
Такое расхождение диагноза объясняется полным крововозмещением и отсутствием на аутопсии у части больных анемии и источника кровотечения. Поэтому при диагностике причины смерти от кровотечения клинические данные приобретают первостепенное значение.
Несмотря на спорность вокруг вопроса о причинах кровотечения, мы попытались выделить основные причины кровопотери у наших больных: плохой гемостаз и прорезывание швов — 23, нарушение свертывающей системы крови—18, парез капилляров и падение сосудистого тонуса — 7, фибринолиз — 2, комплекс причин — 6, причина неизвестна — 10. Неизвестная причина кровотечения была при достаточном гемостазе и нормальной коагулограмме.
По поводу внутриплевральных кровотечений сделано всего 18 реторакотомий, причем у двух больных источник кровотечения не найден, хотя в дальнейшем кровотечение прекратилось. Источниками кровотечения у 16 больных были: стенка желудочка — 3, стенка предсердия — 2 (прорезывание швов), межреберная артерия — 3, кровотечение из анастомоза аортолегочного — 4, спайки — 2, внутренняя грудная артерия — 1 (соскочила лигатура), легочная артерия — 1 (повреждена стенка во время операции). В 11 случаях реторакотомия была своевременна и кровотечение остановлено.
У 7 больных реторакотомия оказалась неэффективной из-за поздней диагностики кровотечения и неправильной тактики лечения.
Консервативная терапия, включающая прямое переливание крови, фибриногена, тромбоцитарной массы, аминокапроновой кислоты, гемофобина и пр., была эффективна у 52 больных, т. е. у большинства. Однако у 13 больных смерть наступила от присоединившейся сердечно-сосудистой слабости, почечно-печеночной или легочной недостаточности. Патогенетическая терапия, которую мы проводим, дает, как правило, благоприятный результат.
Для правильной оценки состояния и принятой тактики борьбы с кровотечением необходимо учитывать особенность и тяжесть дооперационного состояния, операционный период — травматичность операции, кровопотерю и ее причины, нейтрализацию гепарина и пр. Следует особенно опасаться кровотечения у больных с «синими пороками» сердца, у которых в крови высокое содержание гемоглобина и эритроцитов. Опасность кровотечения представляют больные, оперированные в условиях «открытого» сердца с длительным ИК. В послеоперационном периоде, особенно в первые сутки, в случае ухудшения состояния прежде всего необходимо исключить наличие кровотечения.
— Читать далее «Метаболизм в условиях гипотермии. Биохимия и ионы эритроцитов при врожденных пороках сердца»
Оглавление темы «Метаболизм на фоне искусственного кровообращения и гипотермии»:
- Кровоточивость при искусственном кровообращении. Кровотечения на фоне гемоделюции
- Гемостаз после операции с искусственным кровообращением. Снижение кровоточивости после ИК
- Частота кровотечений в кардиохирургии. Кровотечения после операции на сердце
- Метаболизм в условиях гипотермии. Биохимия и ионы эритроцитов при врожденных пороках сердца
- Адениловые нуклеотиды эритроцитов при гипотермии. АТФ-азная активность эритроцитов при гипотермии
- Морфология эритроцитов при искусственном кровообращении. Функция эритроцитов при ИК
- Метаболизм после искусственного кровообращения. Обмен веществ после ИК
- Энергетические процессы после коррекции порока сердца. Ранний послеоперационный период коррекции ВПС
- Метаболизм при тетраде Фалло. Нарушения кровообращения при тетраде Фалло
- Нарушения метаболизма миокарда. Сердечная недостаточность после операции на сердце
Источник
Резюме. Приведены рекомендации по профилактике и снижению риска периоперационной кровопотери в кардиохирургии. Описан алгоритм по переливанию крови и ее компонентов для восстановления гемостаза у оперированных пациентов
 Сердечно-сосудистая хирургия, как правило, связана с периоперационной потерей крови и высокой потребностью ее переливания в послеоперационный период. Контроль кровопотери во время оперативных вмешательств и своевременное возмещение имеющихся потерь во время кардиохирургического вмешательства способствует поддержанию периоперационного гемостаза, снижает риск необоснованного кровотечения и уменьшает потребность в переливании аллогенной крови. Адекватный контроль периоперационной кровопотери во многом зависит от слаженной работы кардиохирурга, кардиоанестезиолога и техника-перфузиолога. Необходимо учитывать также специфику данной отрасли медицины, которая немыслима без искусственного кровообращения, что отличает эту дисциплину от других хирургических специальностей.
Сердечно-сосудистая хирургия, как правило, связана с периоперационной потерей крови и высокой потребностью ее переливания в послеоперационный период. Контроль кровопотери во время оперативных вмешательств и своевременное возмещение имеющихся потерь во время кардиохирургического вмешательства способствует поддержанию периоперационного гемостаза, снижает риск необоснованного кровотечения и уменьшает потребность в переливании аллогенной крови. Адекватный контроль периоперационной кровопотери во многом зависит от слаженной работы кардиохирурга, кардиоанестезиолога и техника-перфузиолога. Необходимо учитывать также специфику данной отрасли медицины, которая немыслима без искусственного кровообращения, что отличает эту дисциплину от других хирургических специальностей.
Эти рекомендации разработаны при совместном участии Европейской ассоциации кардиоторакальной хирургии (EACTS) и Европейской ассоциации кардиоторакальных анестезиологов (EACTA) и являются базовыми для использования в кардиохирургии взрослых для контроля и возмещения кровопотери. Они помогут всем причастным к работе в кардиохирургии врачам оперативно решать вопросы контроля гемостаза на всех этапах лечения, позволят оптимизировать предоперационную профилактику коагулопатий и лечение нарушений, вызванных кровопотерей.
Известно, что кардиохирургия связана с высоким риском периоперационной кровопотери, высокой потребности переливания крови в связи с применением аппарата искусственного кровообращения на фоне общей гепаринизации для поддержания состояния гипокоагуляции. Частая потребность в переливании крови, как и повторная операция в связи с возникшим кровотечением, таит в себе риск неблагоприятного исхода. Внедрение мультидисциплинарной программы по контролю за гемостазом пациента на всех этапах кардиохирургического вмешательства может значительно сократить риск периоперационных кровотечений и надобность в переливании крови, что положительно отразится на результатах лечения.
Известные на сегодняшний день рекомендации по восполнению кровопотерь при проведении оперативных вмешательств имеют существенные различия и не предполагают единого терапевтического подхода. Хотя все предложения едины в том, что первым шагом на пути оптимального решения является выявление пациентов с высоким риском кровотечения и потребности в переливании крови, а также риска повторных оперативных вмешательств. Кроме того, существует небольшой консенсус относительно того высокого риска развития неблагоприятных осложнений при массивных переливаниях аллогенной крови.
Настоящие рекомендации, разработанные совместно Обществом кардиоторакальных хирургов и кардиоторакальных анестезиологов (EACTS и EACTA), которые являются первой попыткой систематизировать имеющиеся знания в области гемостазиологии в кардиохирургии и облегчить предоперационное прогнозирование потребности в переливании крови, опубликованы в «European Journal of Cardio-Thoracic Surgery» («Журнал Европейского общества кардиоторакальных хирургов») в 2017 г.
Основные положения изложены ниже.
Предоперационная лабораторная диагностика нарушений гемостаза
Неадекватное выявление пациентов, имеющих повышенный риск кровотечения на дооперационном этапе, чревато развитием интраоперационной анемии и кровотечения. Поэтому предоперационный контроль включает оптимизацию тромбопрофилактики, уровня гемоглобина с учетом сопутствующих заболеваний и площади поверхности тела, а также выявление врожденных и приобретенных дефектов гемостаза.
Контроль лабораторных показателей
На сегодня наиболее часто выявляемым фактором риска послеоперационного кровотечения является низкий уровень фибриногена. Можно ожидать, что низкий предоперационный уровень фибриногена и тромбина ассоциируется с высоким риском кровотечения, особенно при операциях на аорте либо в ургентном порядке.
Несмотря на распространенное частое определение в предоперационный период коалологических тестов, таких как протромбиновое временя и активированное частичное тромбопластиновое время, нет четкой корреляции с риском развития периоперационного кровотечения.
В тоже время снижение уровня тромбоцитов <100·10–9/л связано с повышенным риском периоперационной кровопотери и необходимостью переливания крови, особенно у пациентов, получающих двойную антитромбоцитарную терапию. Рекомендации относительно коррекции антитромботической терапии у пациентов, требующих кардиохирургического вмешательства, приведены в табл. 1.
Таблица 1. Предоперационная коррекция приема антикоагулянтов и антиагрегантов
| Рекомендации | Класс доказательства | Уровень |
|---|---|---|
| Пациентам, которым показано аортокоронарное шунтирование (АКШ), необходимо получать ацетилсалициловую кислоту до момента проведения хирургического вмешательства | IIa | С |
| Пациентам с высоким риском кровотечения или показанием к переливанию крови, не требующим экстренного хирургического вмешательства, ацетилсалициловую кислоту отменяют за 5 дней до предстоящей операции | IIa | С |
| Возобновление приема ацетилсалициловой кислоты необходимо начать спустя 24 ч при отсутствии кровотечения после изолированного проведения АКШ | I | B |
| У пациентов, получающих двойную антитромбоцитарную терапию и не нуждающихся в экстренном хирургическом вмешательстве, операция возможна через 3 дня после отмены тикагрелола, через 5 дней — клопидогреля и на 7-й день после отмены прасугреля | IIa | B |
| Прекращают прием ингибиторов гликопротеиновых рецепторов GPIIb/IIIa за 4 ч до операции | I | C |
| Для снижения риска кровотечения у пациентов, получавших пероральные антикоагулянты, они могут быть заменены на гепарин — низкомолекулярный либо нефракционированный — у лиц с высоким риском тромботических осложнений | I | B |
| Рекомендуется прекратить профилактическое применение низкомолекулярных гепаринов за 12 ч, а фондапаринукса — за 24 ч до оперативного вмешательства. Интервал может быть увеличен при наличии почечной недостаточности | I | B |
| Рекомендовано заменить прием пероральных антикоагулянтов на нефракционированный гепарин | I | B |
| Те пациенты, кому пероральные антикоагулянты заменили на подкожное введение низкомолекулярного гепарина, как альтернативу могут применять нефракционированный гепарин | IIa | B |
| Плановую кардиохирургическую операцию можно проводить при международном нормализованном отношении (МНО) ≤1,5 у пациентов, получавших препараты антагонистов витамина К. Когда же оперативное вмешательство отложить невозможно, коагуляционная активность восстанавливается | IIa | C |
| Пациенты, требующие планового хирургического вмешательства и принимающие пероральные прямые антикоагулянты, должны прекратить их прием за 48 ч до операции. Этот интервал может быть увеличен при наличии почечной недостаточности | IIa | C |
Коррекция предоперационной анемии
Анемия является частым сопутствующим заболеванием у пациентов пожилого возраста. В легкой форме ее отмечают у 40% пациентов. Снижение гемоглобина в крови ≤100 г/л наблюдается при тяжелой анемии и является предиктором неблагоприятного исхода оперативного вмешательства и повышенной потребности в переливании крови в послеоперационный период. Для профилактики неблагоприятных исходов при наличии анемии рекомендуется применять эритропоэтин с добавлением железа или без него в предоперационный период, что позволит снизить потребность послеоперационного переливания крови.
Рутинно переливание крови для коррекции анемии в предоперационный период не проводится.
Однако в случае экстренной операции и жизнеугрожающей анемии ее переливание обосновано!
Периоперативные мероприятия по снижению потребности в переливании крови.
Интраоперационное поддержание гемостаза является мультидисциплинарной и многофакторной задачей. Тем не менее тщательный гемостаз, минимальная гемодилюция, нормотермия, малотравматичные вмешательства с применением техники операций на работающем сердце или мини-инвазивных технологий позволят значительно снизить риск кровопотери и потребность в переливании крови.
Применение систем с минимальным объемом заполнения (≈600–750 мл) для обеспечения искусственного кровообращения с антитромботическим покрытием дает значительное преимущество на пути кровесберегающих технологий, хотя и не снижает риска повторных операций.
Пассивные гемостатические агенты, активирующие тромбоциты, включая коллаген, желатины и регенерированную окисленную целлюлозу, имеют ограниченное значение.
С учетом имеющихся данных рутинное применение местных герметиков при кардиохирургических вмешательствах не рекомендуется и может быть рассмотрено только в случае стойкого кровотечения для его локализации.
Показания для реинфузии аутокрови
Имеющиеся данные литературы подтверждают, что реинфузия аутокрови уменьшает потребность в переливании аллогенной крови во время кардиохирургических вмешательств.
Но при этом повышается риск развития системного воспалительного ответа, поскольку в собранной крови содержатся высокие концентрации воспалительных медиаторов, продуктов расщепления фибрина, интерлейкинов, жировых частиц и лейкоцитов, увеличивающих воспалительный ответ. Поэтому необходимо помнить об этом при рутинном аутопереливании. Переливание более 1000 мл аутокрови может привести к нарушению коагуляционных свойств крови.
В целом применение собранной крови в виде отмытых эритроцитов и пропущенной крови через систему лейкоцитарных фильтров (система селсейвер) способно уменьшить провоспалительный ответ и количество переливаний у пациентов с кровотечением.
Ультрафильтрация
Общий объем крови во время искусственного кровообращения можно контролировать с помощью ультрафильтрации. Это достигается при окончании периода искусственного кровообращения в результате возврата перфузата, лишенного избыточной жидкости.
Хотя в большинстве исследований было отмечено положительное влияние ультрафильтрации на послеоперационные потребности в переливании крови, особенно при наличии предоперационной анемии, данные основаны на небольших исследованиях.
Влияние гипотермии и рН на гемостаз
Процесс коагуляции имеет ферментативный характер и требует оптимальной температуры и уровня кислотности. Поэтому гипотермия и ацидоз, без которых невозможна кардиохирургия, способны ухудшать гемостаз. Даже умеренная степень ацидоза (pH <7,35) и гиперлактатемия (лактат >4,0 ммоль/л) были связаны со значительно большим объемом экссудата в послеоперационный период.
Таким образом, несмотря на отсутствие крупных проспективных исследований по регулированию температуры и поддержанию рН во время кардиохирургических вмешательств, существует общее согласие, что система коагуляции требует поддержания физиологических параметров, включающих нормотермию и рН ≈7,4.
Интраоперационное поддержание коагуляции
Гепарин связывается с антитромбином, который потенцирует инактивацию тромбина, фактора Xa и антитромбина до 1000 раз. Чувствительность к гепарину индивидуальна у каждого пациента и оценивается с помощью теста на активированное время свертывания (АВС). Целевые значения АВС варьируются от 300 до 600 с. Остаточный гепарин в крови на момент окончания операции в значительной степени способствует риску послеоперационного кровотечения. Его нейтрализация проводится путем должной дозы протамина, введенной в конце операции.
Таким образом, оптимальный уровень гепаринизации необходимо контролировать путем определения величины АВС.
Нейтрализацию остаточного гепарина в крови проводят путем введения протамина в соотношении 1:1 к исходному болюсу гепарина.
Дооперационное депонирование аутокрови
Имеющиеся данные позволяют рекомендовать предоперационное депонирование крови с последующим ее возмещением у пациентов после кардиохирургического вмешательства. Прежде всего у пациентов с аортальным стенозом (средняя степень тяжести), ишемической болезнью сердца (3–4 степень), острым коронарным приступом в анамнезе более 4 нед при высоком уровне гемоглобина (>110 г/л), которым показана плановая хирургия.
Нормоволемическая интраоперационная гемодилюция
Замещение и депонирование крови во время операции, которая заменяется равным объемом коллоидно-альбуминового или кристаллоидного раствора, — оправдано.
Доказано благотворное влияние на показатели послеоперационного гемостаза и на снижение частоты переливания крови.
Снижение риска послеоперационного фибринолиза
Антифибринолитическую терапию широко используют для снижения риска хирургического кровотечения, частоты переливаний продуктов крови и повторных операций в связи с кровотечением. На сегодня наибольшее применение имеют транексамовая кислота, апротинин и аминокапроновая кислота. Хотя апротинин был выведен с рынка в 2007 г., в некоторых странах препарат остается востребованным.
Аминокапроновая кислота — снижает риск переливания крови (ОР 0,70; 95% ДИ 0,52–0,93; р=0,015), но не снижает риск повторных кровотечений.
Транексамовая кислота — по сравнению с плацебо у пациентов, которым выполняли АКШ, снижает риск повторной операции из-за значительного кровотечения (ОР 0,36; 95% ДИ 0,21–0,62; р <0,001) и уменьшает необходимость переливания любых продуктов крови (37,9% против 54,7%; р<0,001). Но необходимо помнить о возможности такого побочного эффекта, как судорожный синдром!
Апротинин
Применение апротинина у пациентов в кардиохирургии изучено широко. Доказана его эффективность в снижении риска повторных операций в связи с кровотечением (ОР 0,46; 95% ДИ 0,34–0,63; р<0,001) и снижении надобности в переливании крови (ОР 0,68; 95% ДИ 0,63–0,73; р<0,001). Тем не менее в связи с повышенным риском летальных исходов у пациентов после АКШ препарат был временно ограничен к применению с 2007 г. Но проведенные в последующем исследования (2012 г.) в Канаде и Европейском Союзе эти утверждения не подтвердили.
Свежезамороженная плазма крови и другие факторы свертывания
Свежезамороженную плазму крови можно использовать для нейтрализации патологических эффектов на гемостаз, вызванных пероральными антикоагулянтами, или в случае непрекращающегося периоперационного кровотечения. Но ее применение в профилактических и терапевтических целях не обосновано, а снижение частоты переливания крови не доказано.
Концентрат фибриногена
Профилактическое введение фибриногена не рекомендуется для снижения риска послеоперационного кровотечения и последующих трансфузий. Тем не менее у пациентов с низким уровнем фибриногена и признаков стойкого микрососудистого кровотечения замещение фибриногена можно рассматривать как снижение потребности в переливаниях.
Факторный комплексный концентрат
В Европе доступны только 4 факторных концентрата, содержащих факторы свертывания II, VII, IX и X. Хотя концентрация фактора IX стандартизирована, другие факторы могут варьироваться в зависимости от разных доступных продуктов. У пациентов с чрезвычайно высокими значениями МНО (>4–5), принимающих антагонисты витамина К в течение длительного времени и нуждающихся в срочной или неотложной хирургии, применение тромбоконцентрата может быть более эффективно, нежели переливание свежезамороженной плазмы крови.
В табл. 2 в приведен краткий алгоритм принятия решения для профилактики и лечения при возникших нарушениях гемостаза и показаний к трансфузии на различных этапах кардиохирургического вмешательства.
Таблице 2. Алгоритм периоперационной коррекции кровопотери при кардиохирургических операциях
| До операции | В процессе операции | Послеоперационный период | |||
|---|---|---|---|---|---|
| Выявление пациентов с высоким риском кровотечения | Контроль и поддержание гемостаза и минимизация кровопотери | Лечение при капиллярном кровотечении после искусственного кровообращения | |||
| Железодефицитная анемия | Пероральный или в/в прием препаратов железа для усиления эритропоэза | Тщательный хирургический гемостаз | Периоперативное лечение при кровотечении согласно протоколу | Определение лабораторных тестов гемостаза на всех этапах лечения | |
| Нежелезодефицитная анемия (недостаток витамина D или фолиевой кислоты) | Эритропоэтин+/—Fe | Минимальная гемодилюция | Минимальный объем заполнения контура аппарата искусственного кровообращения, дооперационное депонирование и послеоперационный возврат крови | Снижение фибриногена (1,5 г/л) либо рыхлый сгусток | Переливание концентрата фибриногена |
| Индивидуальный подбор дозы гепарина и протамина | Введение гепарина либо низкомолекулярного гепарина по величине АВС | Дефицит факторов коагуляции (удлинение времени образования сгустка) | Концентрат протромбина или свежезамороженная плазма крови | ||
| Поддержание нормотермии (≥36 ˚С) и физиологического pH (7,35–7,45) | Согрев пациента и инфузия подогретых растворов | Снижение уровня тромбоцитов (<50·109/л) или на фоне приема антитромбоцитарных препаратов | Переливание тромбоконцентрата или назначение десмопрессина | ||
| Определение уровня фибриногена | Предотвращение фибринолиза | Применение транексамовой кислоты, апротинина, аминокапроновой кислоты | Анемия | Переливание эритроцитарной массы в зависимости от состояния пациента | |
| Определение функциональной способности тромбоцитов у пациентов, получающих ингибиторы гликопротеиновых рецепторов GPIIb/IIIa или же двойную терапию | Сбор крови периоперационных потерь с использованием системы селсейвер | ||||
- Pagano D., Milojevic M., Meesters M.I. et al. (2017) EACTS/EACTA Guidelines on patient blood management for adult cardiac surgery. Eur. J. Cardio-Thoracic Surgery, 53(Issue 1): 79–111.
Александр Осадчий
Источник


