Остановка кровотечения при повреждениях печени
Операции при повреждении печени. Методы остановки кровотечений из печени.
При небольших поверхностных разрывах печени для выполнения гемостаза применяют П-образные швы, накладывая их в поперечном направлении по отношению к сосудам и желчным протокам печени. Для наложения швов на паренхиму печени применяют викрил или кетгут № 4 на атравматичной игле. В случае отсутствия атравматичного материала возможно использование круглой иглы с нитью № 4 или № 6. Применять нерассасывающийся шовный материал для наложения швов на ткань печени нельзя, так как в этом случае наблюдаются длительная воспалительная реакция и нередко абсцедирование, которое требует повторной операции и удаления шовного материала, являющегося инородным телом.
При разрывах печени глубиной более 3 см выполняют иссечение краев и удаление нежизнеспособных участков ткани, а затем на обе стороны дефекта накладывают гемостатические П-образные швы, отступая от края раны не меньше чем на 0,5 см. После достижения гемо- и желчестаза края дефекта сближают послойным наложением непрерывных или П-образных узловых швов, заходя за линию гемостатических швов (отступая от края раны не меньше чем на 1 см) и используя их для уменьшения нагрузки на рыхлую ткань печени. Швы следует затягивать осторожно, чтобы избежать их прорезывания. Для этого ассистент хирурга обеими руками старается максимально сблизить края разрыва. При прорезывании гемостатических швов под них подкладывают синтетические рассасывающиеся пленки При невозможности сближения краев раны или прорезывании швов дефект ткани тампонируют прядью сальника и узлы завязывают сверху этой пряди. При этом следует избегать травматизации или захватывания в шов сосудов, питающих прядь большого сальника. При наличии ран в области серповидной связки дефект можно укрыть мобилизованной серповидной связкой.
При закрытой травме печени наблюдаются самые разнообразные повреждения печени — от небольшого разрыва свободного края до разделения органа на фрагменты (с различной степенью жизнеспособности) Наиболее часто встречаются неправильной формы разрывы капсулы и паренхимы с истечением крови и желчи (60— 70 %), Размозжение нескольких сегментов, напротив, встречается всего в 1—2 ‘, случаев Нередко при закрытой травме живота хирург встречает большие подкапсульные гематомы, представляющие собой разрыв паренхимы с сохраненной капсулой (15—20 %). Подкапсульная гематома выглядит как флюктуирующее плоское образование темного цвета, расположенное под капсулой Глиссона. Ввиду большой вероятности двухэтапного разрыва такие гематомы следует опорожнить, осуществляя гемостаз одним из вышеуказанных способов. Особую форму закрытой травмы печени представляют внутрипеченочные гематомы (10—12 %), которые трудно диагностировать даже во время лапаротомии, так как внешний вид печени может не меняться. Косвенными внешними признаками внутрипеченочной гематомы могут быть участок кровоизлияния темного цвета или небольшая звездчатая трещина капсулы. В любом случае внутри печеночная гематома подлежит консервативному лечению и динамическому наблюдению.
При наличии глубоких трещин печени без повреждений крупных сосудов необходимо использовать гепатопексию с целью создания замкнутого изолированного пространства. Гепатопексия по Хиари — Алферову — Николаеву показана также при наличии ран или разрывов на диафрагмалыюй или нижнедорсальной поверхности печени. Операция заключается в фиксации свободного края соответствующей доли печени от круглой до треугольной связки с диафрагмой по линии ее прикрепления к грудной стенке (при разрывах диафрагмальной поверхности печени) или с задним листком париетальной брюшины (при наличии травмы по нижней поверхности). После такой операции искусственно создается замкнутое щелевидное пространство емкостью 15—25 мл, при этом к линии швов в поддиафрагмальное или подпеченочное пространство для оттока раневого отделяемого подводят двухпросветиыс дренажи.
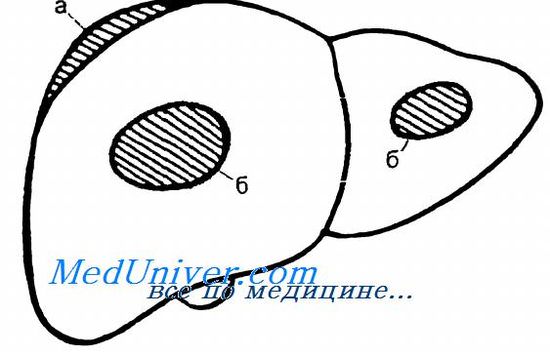
Схематическое расположение подкапсульной (а) и внутрипеченочной гематом (б).
При разрывах печени, сопровождающихся профузным кровотечением, изложенными выше приемами не всегда удастся добиться полного гемостаза, особенно при значтслкном разрушении ее паренхимы и при наличии гемобилии. В таких случаях, если при временном пережатии геиатодуодснальной связки имеется достаточный гемостатический эффект, печеночную артерию перевязывают. Для этого диссектором по верхнему краю гепатодуоденальной связки выделяют общую печеночную, собственную печеночную и пузырную артерии Собственную печеночную артерию перевязывают викрилом дистальнее места отхождения пузырной артерии (в противном случае возможно развитие некроза стенок желчного пузыря, и тогда потребуется холецистэктомия). Необходимо подчеркнуть, что перевязка печеночной артерии сама по себе приводит в 20—25 % случаев к летальным исходам за счет развития множественных мелких сегментарных некрозов, поэтому данный прием следует использовать при крайней необходимости.
У пострадавших с повреждением печени IV степени по Мооге паренхима печени представлена отдельными фрагментами, имеющими связь друг с другом только сосудисто-секреторными ножками. Удаление таких фрагментов не представляет сложности после раздельной перевязки сосудов и желчных протоков. Раневую поверхность печени в таких случаях прикрывают прядью большого сальника и фиксируют его к капсуле печени отдельными швами.
Травмированные участки печени с сомнительной жизнеспособностью необходимо удалять, начиная из глубины разрыва. При этом пальцами тупо разделяют участки ткани, ощущая натягивание кровеносных сосудов и желчных протоков (этот прием называется дигитоклазией), а затем прошивают и перевязывают викрилом сосуды и протоки.
При глубоких и кровоточащих разрывах для достижения гемостаза производят частичное разделение печени по ходу портальных щелей. Для этого ассистент осторожно разводит края печени, а хирург пальцами левой руки постепенно выделяет в паренхиме в зоне повреждения сосуды и желчные протоки, следуя по ходу сосудисто-секреторного пучка. Обнаружив источник кровотечения, сосуд вместе с прилежащим участком паренхимы печени прошивают обвивным викриловым или кетгутовым швом на атравматичной игле.
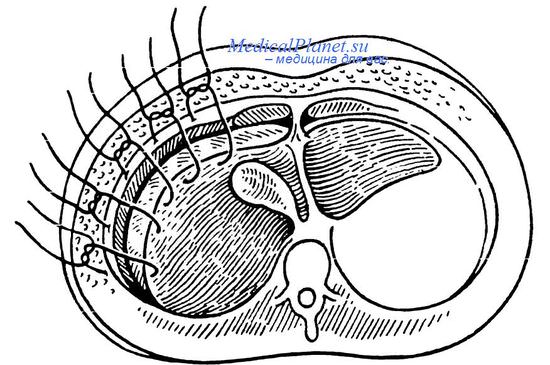
Гепатопексия по Хиари-Алферову-Николаеву.
После окончательной остановки кровотечения из печени постепенно ослабляют турникет с гепатодуоденальной связки, при этом в течение 10—15 мин наблюдают за изменением окраски печени. Появление темно-багрового или серого цвета свидетельствует о нарушении кровоснабжения и требует удаления соответствующего сегмента, однако при большой кровопотере, нестабильной гемодинамике это технически сложное и травматическое вмешательство следует отложить на 2—3 сут до стабилизации состояния или до доставки пострадавшего в специализированный стационар. Необходимо помнить, что выполнение таких расширенных вмешательств приводит к резкому увеличению леальности (до 60-80 %).
При невозможности выделения сосудисто-секреторных ножек и продолжающемся кронетечении из печени как исключение можно применить тугую тампонаду раны, используя 5-6 марлевых тампонов, которые выводят через контрапертуру в правом подреберье.
При обширных повреждениях обеих долей печени и профузном кровотечении также вынолняют тугую тампонаду марлевыми тампонами. Во всех случаях тяжелой травмы печени, в том числе и при тугой тампонаде, показаны дренирование двухпросветными силиконовыми трубками поддиафрагмального и подпеченочного пространств и обязательная декомпрессия желчевыводящих путей путем наружного дренирование холедоха по Керу или, в крайнем случае, наложения холецистостомы.
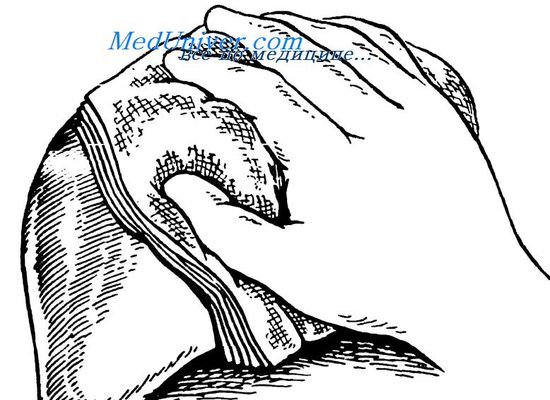
Тугая тампонада разрыва печени
Таким образом, оперативному лечению подлежат любые повреждения печени при продолжающемся кровотечении в брюшную полость. Применяемые при этом способы гемостаза зависят от опыта хирурга, технического оснащения операционной и характера повреждении печени.
Объем вмешательства на печени должен быть максимально щадящим, имея своей целью достижение темо- и желчестаза. Эффективным является применение как физических (электрическая, ультразвуковая, лазерная коагуляция), так и химических (фибриновый клей, тахокомб и др.) методов.
Обширные разрывы и глубокие раны паренхимы печени с повреждением сегментарных сосудисто-секреторных образовании требуют полноценной хирургической обработки с удалением нежизнеспособных тканей и отдельным лигированием кровеносных сосудов и желчных протоков. В случае неэффективного гемостаза могут быть использованы тампонада биологическим материалом, френогепатопексия, а также наружное сдавление печени. Метод наружного сдавления может вызывать резкое нарушение кровоснабжения органа и используется только при наличии определенного опыта.
Обширные первичные резекции печени при ее повреждении сопровождаются чрезвычайно высокой летальностью и не могут быть рекомендованы в широкую клиническую практику, тем более при тяжелой сочетанной травме.
— Также рекомендуем «Операции при повреждении селезенки. Методы остановки кровотечений из селезенки.»
Оглавление темы «Операции на паренхиматозных органах при сочетанной травме.»:
1. Оперативный доступ при сочетанной травме. Временный гемостаз и эвакуация крови при сочетанной травме.
2. Ревизия органов брюшной полости при сочетанной травме.
3. Реинфузия крови при сочетанной травме.
4. Операции при повреждении печени. Методы остановки кровотечений из печени.
5. Операции при повреждении селезенки. Методы остановки кровотечений из селезенки.
Источник
Для временной остановки кровотечения могут использоваться пальцевое сдавление печени, наложение на нее эластических зажимов, временное сдавление печеночнодвенадцатиперстной связки.
Последний способможет применяться не более 15 мин из-за угрозы некроза печени, венозного стаза с кровоизлияниями в органах желудочно-кишечноготракта и явлений коллапса. Сдавление печеночнодвенадцатиперстной связки производят пальцами левой руки или специальным зажимом.
Для окончательной остановки кровотеченияиз паренхимы печени предложены механические, физические, химические, биологические способы, а также специальные гемостатические препараты.
Наиболее просты и надежны механические способы: наложение печеночного шва, перевязка сосудов в ране, тампонада раны.
Среди специальных печеночных швов следует отметить шов Кузнецова — Пенского, Оппеля и др. (рис. 240).
Сущность шва Кузнецова — Пенского заключается в прошивании печеночной ткани через всю толщу двойной лигатурой, которую попеременно выводят на верхнюю и нижнюю поверхности печени и не затягивают.
Одну из нитей в местах выхода ее на поверхность пересекают, а затем концы отдельных смежных нитей связывают между собой и затягивают. Благодаря этому вся печеночная ткань оказывается стянутой рядом отдельных швов над капсулой. Удобным, простым и надежным является наложение обычных матрацных швов с проведением их через сальник, которым окутывают печень. Использование сальника на ножке предотвращает прорезывание швов и обеспечивает гемостаз.
Джиардано прошивает паренхиму печени отдельными двойными нитями. После рассечения нитей концы их связывают на верхней и нижней поверхностях печени.
В. А. Оппель применял цепочный шов, состоящий из отдельных матрацных швов, нити которых связывают между собой.
Н. А. Рубанова предложила строчечный шов, который заключается в том, что паренхиму печени прошивают длинной кетгутовой нитью по типу матрацного шва вначале в одном направлении, а затем, возвращаясь обратно, — в противоположном направлении.
Для предупреждения прорезывания ткани печени можно перед наложением матрацных швов край печени окутать полоской, выкроенной из сальника, фасции или синтетических материалов (капрон, лавсан и др.).
Изолированная перевязка сосудов применяется в качестве дополнения к печеночному шву.
Из физических методов остановки кровотечения используют горячие компрессы. Марлевую салфетку, смоченную горячим изотоническим раствором хлорида натрия, укладывают на рану печени и туго прижимают в течение 5—10 мин. Иногда используют электрокоагуляцию, однако образующийся при этом на поверхности среза печени струп может расплавиться и отторгнуться, вызвав вторичное кровотечение.
Из биологических методов остановки кровотечения наиболее часто используют тампонаду сальником, обладающим гемостатическими свойствами. Сальник является хорошим пластическим материалом, быстро прирастающим к поврежденной поверхности печени.
В качестве гемостатического препарата дляостановки кровотечения из печени предложены фибринные и коллагеновые пленки и губки.
Способы остановки кровотечения из паренхиматозных органов разделяют на следующие группы:
1. механические (гемостатические швы);
2. физические(электрокоагуляция, лазерное излучение);
3. химические (препараты Са, альфа-аминокапроновая кислота);
4. биологические (препараты крови, гемостатическая губка, фибриновая пленка, тампонада сальником).
С целью временной остановки кровотечения при повреждении печени можно произвести пальцевое пережатие печеночно-двенадцатиперстной связки вместе с находящимися в ней сосудами в течение 10–12 минут.
Для окончательной остановки кровотечения в хирургии печени были предложены различные методы гемостатического шва (М. М. Кузнецов, Ю. С. Пенский, Джиордано, Варламов и др.), усовершенствование которых проводится до наших дней. Все методы основаны на одном принципе: сдавить края кровоточащей раны и наложить лигатуры на крупные сосуды. Наложение линейного шва на рану печени возможно только при небольших краевых повреждениях.
Чтобы избежать прорезывания швов, в ряде случаев используют пластинки фасции, серповидную связку, синтетические ленты, которые накладывают по периметру раны, а затем прошивают их вместе с тканями печени. Для герметизации ран печени применяют подшивание сальника или прикрывают культю печени лоскутом серповидной связки (иногда добиваются герметизации швов линейной раны печени дополнительным наложением слоя цианакрилатного клея).
.
Источник
Травмы паренхиматозных органов диагностируются у 12-50% больных с повреждениями органов брюшной полости, занимая 2-3-е место [1, 5, 11, 17]. Хирургическая тактика при повреждениях печени, селезенки определяется характером травмы и должна быть направлена в первую очередь на обеспечение гемостаза и холестаза [14-16]. Для достижения окончательного гемостаза при ранениях печени и селезенки применяют прошивание, биологические и синтетические пленки, клеевые композиции, методы неконтактного воздействия (лазерная, плазменная, аргоновая и электро-коагуляции) [2-8, 13, 18, 19]. При обширных раневых дефектах печени, селезенки с размозжением ткани выполняют резекции с гемостазом по ходу и с иссечением нежизнеспособных участков паренхимы, по типу первичной хирургической обработки [11, 14]. При отдельных видах травмы печени возможно выполнение оменто- и френогепатопексии. Нередко развиваются некрозы паренхимы печени, селезенки в зоне швов, с развитием нагноений, вторичных кровотечений, желчных свищей, требующих повторных операций [3, 7, 9, 10, 12]. Одной из причин неудач хирургического лечения травм печени и селезенки является отсутствие четких рекомендаций по выбору метода достижения окончательного гемостаза и определения объема вмешательства в зависимости от тяжести повреждения. Совершенствование методов остановки кровотечения при травмах печени и селезенки, а также разработка критериев выбора рациональной тактики при их повреждениях остаются актуальными и по сей день.
Травма печени и селезенки моделировалась в эксперименте на 138 беспородных собаках обоего пола весом от 7 до 20 кг. Смоделировано 268 травм печени и селезенки. Раны наносили с помощью скальпеля, снабженного ограничителем (68): резаные длиной 3 см и более, глубиной не более 2/3 толщины органа (30) и колото-резаные (38). У 38 животных после обеспечения гемостаза первичной раны печени наносили рану селезенке. Тупую травму живота нанесли 26 животным с развитием подкапсульных (20) и внутриорганных (6) гематом. Из них у 13 животных нанесена тупая травма и печени и селезенки. Разрывы печени и селезенки моделировали интраоперационно путем раздавливания паренхимы зажимом по методике Е.С. Владимировой и соавт. [5] у 41 животного; разрывы диафрагмальной и висцеральной поверхностей печени у 20 и селезенки у 21. Размозженные раны доли и сегмента с повреждением интрапаренхиматозных структур смоделированы на 119 животных: селезенки (88) и печени (31) (когда выполняли резекцию органа). Травму ворот селезенки с повреждением ее сосудистой ножки и последующей спленэктомией нанесли 14 животным (см. таблицу).
Все операции выполняли под внутриплевральным тиопенталовым наркозом. Брюшную полость вскрывали верхнесрединным разрезом. Выводили в операционную рану селезенку, печень. При развитии профузного кровотечения накладывали специальное устройство на питающие сосуды соответствующего участка органа (патент РФ на полезную модель РФ №70622) или мягкий эластический жом (патент РФ №2014802) на паренхиму органа, проксимальнее раны или разрыва для обеспечения временного гемостаза. При травмах печени также применили маневр Прингла (пережатие печеночно-двенадцатиперстной связки) или накладывали эластический жгут на паренхиму органа, проксимальнее раны. Раны ушивали хромированным кетгутом (№2-3) или викрилом на атравматичных колющих иглах.
Техника шва при ранах глубиной до 2/3 толщи органа: иглы вкалывали отступя от края раны (а) 1,0 см на расстоянии 1,0-1,5 см между ними, начиная с середины раны (в-в1), с выколом на противоположной стороне под углом 45° (б) к длине раны, направляя иглы кнаружи и в разные стороны. Потом обе иглы переводили поверх раны на первоначальную сторону и строго напротив выкола еще раз на расстоянии 1,0 см от края раны делали вкол под углом 45° к длине раны, направляя иглы к центру раны, выводили их напротив первого вкола. Концы нитей связывали между собой (патент РФ №2346660) (см. рисунок). Рисунок 1. Схема ушивания резаных ран печени и селезенки. а — рана; в-в1 — нити, последовательность проведения.
Рисунок 1. Схема ушивания резаных ран печени и селезенки. а — рана; в-в1 — нити, последовательность проведения. Рисунок 1. Схема ушивания резаных ран печени и селезенки. б — угол, под которым проводится игла; в-в1 — нити, последовательность проведения.
Рисунок 1. Схема ушивания резаных ран печени и селезенки. б — угол, под которым проводится игла; в-в1 — нити, последовательность проведения.
Предварительно шов был использован на изолированных макропрепаратах печени и селезенки с последующим контрастированием внутриорганных структур. Выявлено, что ушивание ран глубиной до 1/3 толщины органа не приводит к выраженному нарушению архитектоники структур (сосудов и желчных протоков), а при ушивании ран глубиной от 1/3 до 2/3 толщины органа могут наблюдаться подобные изменения. Шов предотвращает прорезывание нитей при сближении краев раны и завязывании узлов и обеспечивает гемостаз.
Сквозные ранения органов ушивали следующим образом: проводили прядь сальника через рану на противоположную поверхность органа. Ушивали раны с помощью предложенного или П-образного шва с обеих сторон, захватывая и сальник (рацпредложение №95822).
При тупой травме с развитием подкапсульных гематом паренхиматозных органов малых размеров — диаметром до 3 см (печень — 10, селезенка — 10) и при отсутствии признаков продолжающегося кровотечения проводили миниинвазивное лечение (патент на изобретение РФ №2321427), из-за опасности вторичного разрыва гематом с последующим кровотечением. При гематомах больших размеров и внутриорганных производили атипичную резекцию соответствующего органа. При размозженных ранах, расположенных по краю органа и разрывах, занимающих целую долю или сегмент с повреждением крупных сегментарно-долевых интрапаренхиматозных структур, производили атипичную резекцию соответствующего участка.
При развитии массивной кровопотери наряду с инфузионной терапией осуществляли реинфузию крови. В большинстве наблюдений дренировали брюшную полость. Животные находились под наблюдением до 1 года.
В сроки от 1 нед до 12 мес проводили повторные операции. Макроскопически оценивали состояние селезенки, печени, их цвет, консистенцию. Селезенку удаляли, печень резецировали, проводили гистологическое исследование в сроки 7, 15, 30, 60, 120, 180, 360 сут после операций. Полученные препараты окрашивали гематоксилином и эозином.
При ранах глубиной до 2/3 толщи органа окончательный гемостаз достигнут в 13 наблюдениях из 15 ранений селезенки и в 12 из 15 ранений печени. Гемостаз удалось обеспечить в 16 из 23 и в 11 из 15 наблюдений при сквозных ранениях селезенки и печени соответственно. При продолжающемся кровотечении применяли дополнительные меры гемостаза. Поверхностные разрывы ушивали с захватом дна раны, но с проведением лигатур вне предполагаемой проекции сегментарных сосудов.
При обширных ранах и разрывах после иссечения нежизнеспособных участков паренхимы с целью гемостаза перевязывали (прошивали) сегментарнодолевые артерии и дополнительно накладывали швы с использованием пластических материалов в качестве подкладки у 8 животных с травмой печени и у 10 животных с травмой селезенки. При разрыве диафрагмальной поверхности селезенки в 6 наблюдениях (рацпредложение №05-1303) и печени в 5 наблюдениях на место разрыва укладывали рассасывающуюся гемостатическую марлю и фиксировали орган к брюшине, покрывающей диафрагму. Аналогично этому, при разрыве висцеральной поверхности селезенки у 3 собак на травмы укладывали гемостатическую марлю и фиксировали орган к большой кривизне желудка, проводя швы через его серозно-мышечный слой. У двух животных при разрыве нижнего полюса селезенки использовали метод «наружного сдавления прядью сальника», с фиксированием гемостатической марли с ушиванием.
При разрыве в проекции центральных сегментов печени глубиной около 2/3 толщи органа производили «поэтажное» ушивание с использованием пластических материалов, перевязкой кровоточащих сосудов in situ и у 2 животных применили ушивание с «наружным сдавлением прядью сальника», рассасывающейся гемостатической марлей. При разрыве висцеральной поверхности печени у 3 животных применили ушивание с использованием гемостатической марли, ТахоКомба и у одного животного для достижения окончательного гемостаза пришлось перевязывать долевую артерию печени.
В общей сложности, резекцию селезенки произвели у 88 собак в 3 сериях. В первой серии резецировали верхний полюс и раневую поверхность укрывали сальником (30 собак). Во второй серии — нижний полюс и раневую поверхность укрывали париетальной брюшиной (23 собаки). В третьей серии резецировали 2/3 органа и рану укрывали рассасывающейся гсмостатической марлей (35 собак). Резекцию печени произвели у 31 собаки также в трех сериях. В первой серии выполнили атипичную резекцию после предварительного прошивания паренхимы гемостатическим швом по границе резекции (8 собак). Во второй серии резекция печени произведена после выполнения маневра Прингла (8 собак). В третьей серии резецировали печень (15 животных), и среди них с использованием жома у 8 собак: предварительно прошивали паренхиму органа через прорези жома гемостатическим швом, отсекали удаляемую часть по краю жома и перитонизировали раневую поверхность органа. Резецированную поверхность укрывали сальником (15 наблюдений), париетальной брюшиной (6 наблюдений), рассасывающейся гемостатической марлей (10 наблюдений). Дополнительные швы вынуждены были наложить при резекциях селезенки у 12 животных и у 7 — перевязывали сосуды в плоскости резекции с помощью разработанного устройства (решение о выдаче патента на полезную модель РФ №2008124330/22(029510)). При резекции печени накладывали дополнительные швы и перевязывали сосудисто-протоковые структуры в плоскости резекции у 9 собак. Резекция печени в среднем занимала 15-18 мин, а селезенки 7-10 мин.
Окончательный гемостаз достигнут у 69 (78,4%) животных при резекциях селезенки (25, 18, 26 наблюдений) и 22 (71%) собак при резекциях печени (6, 5, 11 наблюдений) в первой, второй и третьей сериях соответственно.
При повреждении ворот селезенки и сосудистой ножки (14 животных) производили спленэктомию с аутотрансплантацией ткани селезенки в большой сальник (6), предбрюшинную клетчатку (2), забрюшинное пространство (2), в ложе прямых мышц живота (4). Для этого использовали фрагменты паренхимы органа размером 0,3×1,0×2,0 см.
У животных с ушитыми ранами селезенки и печени послеоперационный период характеризовался благоприятным течением. В послеоперационном периоде погибли 14 (10,4%) собак: вследствие невыхода из наркоза — 6 (резекция верхнего полюса селезенки (2), ушивание разрыва селезенки (1), резекция печени (2), ушивание разрыва печени (1)). Спаечная кишечная непроходимость развилась у 3 животных (резекция нижнего полюса селезенки (2), спленэктомия и аутотрансплантация в большой сальник (1)). Послеоперационный перитонит выявлен у 3 собак (резекция 2/3 селезенки (1) резекция печени (1), ушивание разрыва висцеральной поверхности печени (1)). Кишечное кровотечение отмечено у одной собаки, она погибла на 50-й день после резекции 2/3 селезенки. Одно животное погибло после ушивания разрыва диафрагмальной поверхности печени на 25-е сутки от поддиафрагмального абсцесса. Остальные животные перенесли операцию хорошо.
Морфологические данные, полученные в динамике после операции, свидетельствуют о хорошей регенерации в области оперированной раны.
Клинические наблюдения
Предложенный шов применили в клинической практике при ушивании:
— резаных ран печени (3 наблюдения): длиной до 5 см и глубиной до 2/3 толщины паренхимы 3 и 4 сегментов печени (2 наблюдения), длиной 5,5 см диафрагмальной поверхности правой доли печени без повреждения интрапаренхиматозных структур (один больной);
— резаных ран диафрагмальной поверхности селезенки длиной до 5 см и глубиной до 2/3 толщины органа (2 больных);
— сквозных ран 4 и 5-6 сегментов печени (2 больных) и селезенки (1 больной со сквозной раной, 1 больной с колото-резаной раной нижнего полюса селезенки);
— разрывов печени (4 больным): разрывы до 5,0 см левой доли диафрагмальной поверхности печени (2 пациента), до 5 см диафрагмальной поверхности 5-6 сегментов доли печени (2 наблюдения), из них с тампонадой сальником (3 больных) и рассасывающейся гемостатической марлей (1 больной);
— разрыва диафрагмальной поверхности селезенки размерами до 4,0 см выполнили ушивание с фиксацией к париетальной брюшине.
Атипичные резекции печени с наложением П-образных швов выполнили 2 больным (разрыв до 5,5 см, связанный с травмой живота и размозженная рана левой доли печени размером 4,5 см с повреждением сегментарных внутриорганных структур). Резекцию селезенки выполнили 4 больным (травмы селезенки (3 больных) и киста нижнего полюса (1 наблюдение)). Подкапсульные гематомы около 3,0 см при отсутствии признаков продолжающегося кровотечения лечили миниинвазивно: у 3 больных диафрагмальной поверхности печени (3 и 6 сегменты) и у 1 больной висцеральной поверхности 5 сегмента. Подкапсульные гематомы диафрагмальной поверхности селезенки размерами до 3 см при отсутствии признаков продолжающегося кровотечения лечили миниинвазивным методом у 4 больных (гематомы средней части селезенки — 2 и нижнего полюса — 2). Во всех наблюдениях удалось обеспечить надежный гемостаз.
Разнообразие повреждений печени и селезенки при травме живота определяет сложность выбора рациональной хирургической тактики. Многое зависит от данных интраоперационной ревизии поврежденного органа. После достижения временного гемостаза и эвакуации крови из брюшной полости решающее значение мы придаем оценке характера повреждений. Поверхностные разрывы печени, селезенки ушиваем с захватом дна раны, с проведением лигатуры вне предполагаемой проекции сегментарных сосудов и с фиксацией к линии шва пластического материала для предупреждения прорезывания.
При глубоких разрывах, более 2/3 толщины органа, исключали возможное повреждение крупных долевых (сегментарных) сосудов и протоков [5]. Для достижения гемостаза при разрывах печени, селезенки наряду с ушиванием возможна и изолированная перевязка сегментарных артериальных сосудов. При краевых размозженных ранах и разрывах, занимающих долю или сегмент, производили соответствующую резекцию. При глубоких ранах в области ворот или множественных разрывах селезенки выполняли спленэктомию с имплантацией фрагментов селезенки. Обязательным условием является перитонизация резекционной поверхности печени, селезенки и дренирование зоны вмешательства.
Таким образом, проведенные исследования показали эффективность предложенных способов гемостаза, что позволит улучшить результаты органосохраняющих операций на печени, селезенке при повреждениях.
Источник


