Осложнения туберкулеза легких кровотечение
Туберкулез – очень серьёзное заболевание, возникновение которого может привести к развитию целого ряда осложнений.
- Кровохарканье и легочное кровотечение
- Лечение
- Спонтанный пневмоторакс
- Виды
- Лечение
Кровохарканье и легочное кровотечение
Кровохарканье и легочное кровотечение наблюдаются в основном при деструктивных формах туберкулеза, бронхоэктазах, прикорневых очагах склероза. Особенно часто это осложнение отмечается у больных с циррозом легких.
Все кровохарканье и кровотечения делят на истинные и ложные (псевдокровохарканья). При истинных кровь выделяется непосредственно из легких, а при ложных — из носоглотки, десен, пищевода, желудка. Ложное кровохарканье возникают не во время кашля.
Источником кровохарканья (кровотечения) могут быть легочные и бронхиальные сосуды. Примерно 95% крови в легкие поступает системой легочной артерии, а 5% — бронхиальными артериями. Легочное кровотечение, как правило, возникает именно из бронхиальных сосудов.
По интенсивности выделения крови различают:
- кровохарканье,
- кровотечение,
- профузное кровотечение (кровоизлияние).
Кровохарканье — это откашливание крови отдельными плевками, сгустками или прожилок крови с мокротой. За сутки выделяется около 50 мл крови. Во время кровотечения больной откашливает одновременно 50-100 мл крови. Легочное профузное кровотечение возникает вследствие разрыва крупных сосудов и очень часто заканчивается смертью от удушья (асфиксии) вследствие заполнения бронхов и трахеи сгустками крови.
По количеству одновременно выделенной крови легочные кровотечения делятся на малые (до 100 мл), средние (от 100 до 300 мл), крупные (более 300 мл).
Патогенез. Кровохарканье и легочное кровотечение могут возникать двумя путями:
- нарушение проницаемости мелких сосудов и капилляров легких, обусловленное специфическими воспалительными изменениями в легких, воздействием токсических веществ на стенку сосудов;
- нарушение целостности сосудов, то есть происходит разрыв сосудов. Причиной этого является язва или механический разрыв стенки крупного сосуда, которая часто изменена по типу аневризматических или варикозных узлов.
Факторы, способствующие возникновению кровохарканье и легочного кровотечения:
— Повышение давления в сосудах малого круга кровообращения;
— Нарушение свертывания крови;
— Повышение фибринолитической активности крови;
— Повышение проницаемости стенок сосудов.
Основными признаками кровохарканья, легочного кровотечения являются:
- Кровь из легких выделяется при кашле;
- Кровь имеет ярко-красный цвет;
- Кровь пенистая.
Следует помнить, что кровь, прежде чем выделиться из легких наружу, должна пройти путь через бронхи, трахею, гортань и попасть в ротовой полости. Этот путь кровь может преодолеть только при наличии кашлевых толчков. Вот почему не существует легочного кровохарканья и кровотечения без кашля.
Локализацию источника кровохарканье или кровотечения устанавливают на основании анамнестических данных, аускультации, перкуссии и рентгенологического исследования. Как правило, кровотечение происходит из легкого, в котором обнаруживают деструктивные изменения. Больные часто сами определяют источник кровотечения. При пальпации кожа половины грудной клетки на стороне кровотечения теплее, может ощущаться перемещения кровяных сгустков. Важнейшее значение для определения источника кровотечения, кроме рентгенологического исследования, имеет бронхоскопия. Источником кровохарканье и легочного кровотечения является полости распада, каверны, очаги фиброза, цирротические изменения.
Дифференцировать кровохарканье и легочное кровотечение нужно от кровохарканья и кровотечения из пищевода, желудка, носоглотки. Кровотечение из носа характеризуется выделением темной крови без кашля, которая стекает по задней поверхности глотки. Кровотечение из расширенных вен пищевода начинается внезапно, имеет профузный характер. Кашель отсутствует. При этом у больных диагностируется цирроз печени. Кровь из желудка выделяется при рвоте, темного цвета, имеет вид «кофейной гущи» (за счет примесей содержимого желудка). Иногда, при свертывании крови в желудке, рвотные массы имеют темные сгустки. При кровотечении из язвы желудка наблюдается большое кровотечение с выделением неизмененной крови с рвотными массами. Кроме того, легочное кровотечение обычно меньше по сравнению с желудочным.
Лечение. Гемостатическое лечение должно быть направлено, прежде всего, на болезнь, которая вызвала кровохарканье и легочное кровотечение, то есть туберкулезом легких и на основные факторы возникновения легочного кровохарканья или кровотечения. Больному создают условия максимального физического и психического покоя. В постели больной должен находиться в положении полусидя, что улучшает откашливание мокроты и сгустков крови, накопленных в дыхательных путях. Возможны незначительные активные и пассивные движения во время медицинского обследования (аускультация, рентгенография с помощью передвижного аппарата). Если кровохарканье умеренное, то полный физический покой не обязателен.
У больных туберкулезом значительную роль имеет гипотензивная терапия, которая может способствовать даже большему гемостатическому эффекту, чем лечебное действие препаратов, регулирующих свертывающей системе крови. Гипотензивные средства можно разделить на препараты быстрого и замедленного действия. Назначение препаратов для снижения давления в сосудах легких зависит от объема кровопотери. Так, при кровохарканье и малой легочном кровотечении целесообразно использовать лекарственные средства замедленного действия, а при большой легочном кровотечении — быстрого действия до прекращения выделения крови.
1. Для ускоренного уменьшения давления в сосудах назначают:
• ганглиоблокаторы — пирилен (0,01 г 3 раза в день), темехин (0,001 г 2-3 раза ни день), бензогексоний (0,1 г 3-4 раза в сутки), пептамип (1-2 мл 5% раствора ) подкожно или внутривенно. Введение ганглиоблокаторов контролируют измерением артериального давления. На плечевой артерии оно не должно быть ниже 80 мм рт.ст. Также для гипотензивного эффекта применяют:
• спазмолитические средства — эуфиллин вводят внутримышечно (1 мл 24% раствора) или внутривенно (10 мл 2,4% раствора). В случае непереносимости эуфиллина вводят папаверина гидрохлорид (1-2 мл 2% раствора) внутривенно или подкожно (вызывает длительное расширение сосудов большого круга кровообращения) или гидрированный папаверин — но-шпу (2-4 мл 2% раствора) внутривенно или подкожно. При незначительном кровохарканьи назначают внутрь эуфиллин (0,1-0,2 г) и гидрированный папаверин — но-шпу (0,02-0,06 г) 2-3 раза в сутки;
• противокашлевые средства — кашель может провоцировать кровохарканье вследствие повышения давления в легочной артерии. Для прекращения или уменьшения кашля назначают бромгексин, атровента и т. д. С этой же целью назначают и атропина сульфат (1 мл 0,1% раствора) подкожно, потому что он подавляет кашлевой рефлекс, устраняет бронхоспазм и расширяет сосуды брюшной полости.
2. Для повышения свертываемости крови используют препараты в зависимости от показателей тромбоэластограммы и коагулограммы. При отсутствии этих исследований препаратами выбора являются дицинон, гемофобин, фибриноген или тромбин. Часто сочетают назначения гемофобин с фибриногеном или тромбоплазмином.
• дицинон (этамзилат натрия) — вводят 2-4 мл 12,5% раствора внутримышечно или внутривенно. Препарат участвует в формировании тромбопластина. Действие начинается через 5-15 минут при внутривенном введении и через 1-2 часа — при внутримышечном;
• фибриноген — вводят 250-500 мл внутривенно капельно. Ускоряет переход фибриногена в фибрин; начинает действовать через 30 минут. В стандартных флаконах содержится 2 г сухого фибриногена. Его растворяют в 500 мл изотонического раствора натрия хлорида или 1 г в 250 мл.
• гемофобин — назначают внутрь по 1 ст. ложке 3% раствора 3-4 раза в сутки. Также ускоряет переход фибриногена в фибрин; начинает действовать через 3-6 часов.
• тромбин — по 1-2 мг в 2 мл дистиллированной воды ингаляционным методом. Викасол целесообразно применять при нарушении протромбинообразовательной функции печени. Для остановки кровохарканья и легочного кровотечения внутримышечно вводят сульфокамфокаин (2 мл 10% раствора), который улучшает функцию дыхания и кровообращения.
3. Снижение фибринолитической активности крови. С этой целью проводят корекцию повышенной активности фибринолитических, протеазных ферментов крови, мокроты и и области воспалительного процесса в легких.
Для этого используется:
• е-аминокапроновая кислота (ингибитор фибринолиза) — вводят 5% 100 мл внутривенно капельно (действие начинается через 15-30 мин.), 5% -3-5 мл спрей (действует через 5-10 мин.);
• контрикал (трасилол), ингитрил (гордокс) (ингибитор протеолиза) — по 10 000 — 20 000 ЕД внутривенно капельно (начало дии через 30-45 мин.);
• амбен, гидрокортизон (ингибиторы гиалуронидазы) — 1% — 5 мл Амбене, 12,5-25 мы гидрокортизона вводят внутривенно струйно (препараты действуют через 10- 15 минут).
4. Уменьшение проницаемости стенки легочных сосудов достигают назначением наступление них средств:
• кальция глюконат — 10мл 10% раствора внутривенно или внутримышечно или внутрь. Кальция хлорид вводят только внутривенно (10 мл 10% раствора);
• аскорбиновая кислота — 1,0 г 3-5 раз в день.
Препараты для заместительной терапии: эритроцитарная масса 150-200 мл 2-3 раза в курс, альбумин 20% — 50 мл, 10% — 100 мл, полиглюкин (реополиглюкин, рондекс) — 400- 1200 мл, раствор бикарбоната натрия — 500- 1500 мл.
При рецидивах легочного кровотечения у больных деструктивными формами туберкулеза легких гемостатический эффект достигается внутривенным (капельно) введением лечебной смеси физиологического раствора (300-500 мл), хлорида кальция (10% -5 мл) и гидрокортизона 12,5-25 мг 1-2 раза в сутки.
Современные методы гемостатического лечения достаточно эффективны и позволяют добиться остановки кровохарканья или легочного кровотечения у 95% больных. Если гемостатическое лечение неэффективно, показано хирургическое лечение. Риск операции уменьшается в 10-15 раз, если ее проводить в период временного прекращения легочного кровотечения.
Особое внимание обращают на профилактику и лечение осложнений, возникающих во время легочного кровотечения. Первоочередной становится профилактика асфиксии вследствие закупорки дыхательных путей кровью. Положение больного должно быть полусидя, что способствует улучшению кровообращения и откашливанию крови. В тяжелых случаях отсасывают кровь из трахеи через катетер. Эффективным является проведение лечебно-диагностической бронхоскопии или интубации, дренирование бронхов и отсасывание сгустков крови. В случаях возникновения ателектаза назначают протеолитические ферменты в сочетании с противотуберкулезными препаратами.
Спонтанный пневмоторакс
Спонтанный пневмоторакс (греч. воздух + панцирь, грудь) — патологическое состояние, характеризующееся поступлением воздуха в плевральной полости при отсутствии поражения грудной клетки.
Патогенез. По механизму возникновения выделяют спонтанный и травматический пневмоторакс. Спонтанный пневмоторакс возникает при нарушении целостности висцеральной плевры, а травматический — париетальной.
Спонтанный пневмоторакс, как правило, является осложнением различных заболеваний легких. Но он может развиваться и без наличия патологического процесса в легких. Такой спонтанный пневмоторакс называется идиопатическим. В этом случае причинами спонтанного пневмоторакса может быть закупорка мелкого бронха мокротой или местный бронхоспазм. Возникает клапанный механизм в бронхах, что сопровождается повышением давления в дистальных отделах дыхательных путей. Вследствие этого альвеолы на ограниченном участке перерастягиваются, стенки их и перегородки атрофируются, и образуется буллезная эмфизема, которая затем разрывается. Травматический пневмоторакс развивается вследствие проникающего повреждения грудной клетки.
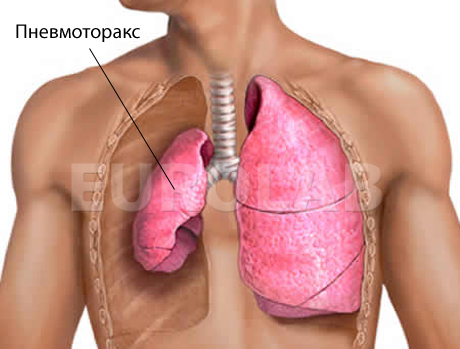
Спонтанный пневмоторакс при туберкулезе легких чаще всего возникает:
а) в результате разрыва буллезной эмфиземы легкого (при фиброзно-очаговом, хроническом диссеминированном туберкулезе легких, пневмосклерозе) или кисты легкого;
б) редко — вследствие прорыва каверны в плевральную щель.
Выделяют следующие виды спонтанного пневмоторакса:
- Открытый — воздух поступает в полость плевры на вдохе и выходит при выдохе через отверстие в висцеральной плевре;
- Закрытый — воздух попадает в плевральную полость при вдохе, но назад не получается, потому что отверстие в висцеральной плевре закрывается;
- Клапанный на вдохе воздух постоянно входит в плевральную пустоту, а на выдохе дефект в висцеральной плевре закрывается, образуя клапан. Клиника спонтанного пневмоторакса в большинстве случаев зависит от размера свободной плевральной полости, вида пневмоторакса и скорости поступления воздуха. Если плевральная полость не облитерированна, ее заполняет воздуха (распространенный пневмоторакс), резко сжимает легкое и органы средостения. Если плевральная полость ограничена (ограниченный пневмоторакс), клинические признаки этого осложнения незначительны.
Больные жалуются на острую боль в пораженной половине грудной клетки, одышку, покашливание. Объективно — тахикардия, тимпанит и ослабленное дыхание на стороне спонтанного пневмоторакса. В случаях ограниченного спонтанного пневмоторакса клинические проявления незначительные, а в тяжелых случаях они настолько характерны, что диагноз можно поставить без рентгенологического исследования. Общее состояние при спонтанном пневмотораксе тяжелое, иногда даже потерей сознания. Больной занимает вынужденное положение — полусидя, становится беспокойным. Появляются симптомы острой недостаточности дыхания, дыхание учащается, становится поверхностным, возникает цианоз, потливость, тахикардия, а в дальнейшем — брадикардия. Смерть больного может наступить от болевого шока или коллапса.
Лечение. Больному придают полусидячее. Вводят омнопон или морфина гидрохлорид для уменьшения боли и угнетения кашлевого центра. Назначают также 2 мл 10% раствора сульфокамфокаина подкожно, оксигенотерапию. Если состояние больного остается тяжелым, проводят пункцию плевральной полости с последующей аспирацией газа к установке отрицательного давления. При аспирации общее состояние больного быстро улучшается, однако затем вновь может ухудшиться, если спонтанный пневмоторакс становится клапанным или открытым.
Если после неоднократной аспирации газа из плевральной полости общее состояние больного ухудшается, рекомендуется проколоть грудную клетку толстой иглой и зафиксировать ее липким пластырем к коже. При этом воздух, который попадает в плевральную полость через поврежденное легкое, будет выходить наружу. Давление в плевральной полости сравнится с атмосферным, вследствие чего легкое и органы средостения не подвергаются сжатию. К игле следует присоединить резиновую трубку, ее конец опустить в дезинфицирующий раствор. Это мероприятие является неотложным в случаях спонтанного пневмоторакса у больных с крайне тяжелым состоянием.
Адекватным методом является дренирование плевральной полости (наложение дренажа по Бюлау) и постоянное отсасывание воздуха. При спонтанном пневмотораксе общее состояние больного удается улучшить консервативными мерами. При неэффективности консервативного лечения ставят вопрос о торакотомии и ушивании поврежденного легкого или резекции легкого.
Источник
Легочное кровохарканье и кровотечение являются частыми симптомами легочной и внелегочной патологии. При туберкулезе легких это одно из наиболее частых осложнений, которое к тому же чревато тяжелыми последствиями для больного.
Кровохарканье и кровотечение могут быть однократными и повторными. Деление легочных кровотечений на кровохарканья и кровотечения целесообразно. Под кровохарканьем подразумевается большая или меньшая примесь крови в мокроте. Это результат диапедеза форменных элементов крови – проявление воспалительного процесса или местного нарушения кровообращения при повышенной проницаемости стенок капилляров и мелких сосудов. Кровотечение представляет собой выделение изо рта жидкой или свернувшейся крови.
В клинической практике чаще используется характеристика кровотечений из легкого, основанная на количестве выделяющейся крови. В основном кровотечения делятся на малые –до 100 мл, средние – до 500 мл и обильные (профузные) – более 500 мл.
При кровохаркании и кровотечении нередко создаются затруднения при определении их источника. Клиническое обследование может установить, что источником кровотечения являются носовая часть глотки, десны, пищевод, желудок.
Выделение крови из носа, носоглотки и полости рта не является истинным кровохарканьем. Подробный опрос больного и обследование полостей носа и рта дают возможность установить причину псевдокровохарканья. При этом больной не откашливает, а в большинстве случаев сплевывает мало измененную по виду кровь без примеси мокроты. При лабораторном исследовании в выделенных «плевках» не обнаруживается элементов мокроты – альвеолярного эпителия. После псевдокровохарканья не наблюдается аспирационных явлений в легких.
При кровотечении из варикозно расширенных вен пищевода чаще диагностируется цирроз печени. Это кровотечение возникает внезапно и носит профузный характер. Кровотечения из язвы желудка сопровождаются рвотой темной кровью с примесью желудочного сока и сгустков крови.
При легочных кровотечениях (истинных) появляются першение в горле, ощущение сдавления, боль за грудиной, удушье, а затем кашель с характерным клокотанием, изо рта выделяется алая, пенистая кровь без сгустков. Профузные легочные кровотечения сопровождаются головокружением, бледностью, тахикардией, снижением артериального давления. Осмотр больного выявляет мелкопузырчатые хрипы в нижних отделах легких на стороне кровотечения, при рентгенологическом обследовании там же может определяться ателектаз или аспирационная пневмония, реже – на противоположной стороне вследствие ретроградного забрасывания крови.
Причиной кровохарканья могут быть пневмонии, рак легкого, актиномикоз легких, эхинококк в легком, пневмокониоз и др. Кровохарканье может быть у лиц, перенесших в прошлом ранения в грудную клетку.
Как ни многочисленны причины кровохарканий и легочных кровотечений, все же наиболее часто они наблюдаются у больных туберкулезом. Кровохарканье может сопровождать как впервые развившийся туберкулезный процесс так и хронические его формы, появляться после заживления участков деструкции, как и при всяком другом пневмосклеротическом процессе.
Кровохарканье у туберкулезных больных в большинстве случаев наступает неожиданно для больного, чаще после инсоляции в жаркие, душные дни, а также при метеорологических колебаниях. Наиболее часты кровохарканья весной и осенью.
Чем же объяснить, что при разрушении легочной ткани, обильно снабженной кровеносными сосудами, кровохарканье встречается примерно у 10 – 15 % больных. Это объясняется тем, что туберкулотоксины при непосредственном действии на сосуды вызывают процессы облитерирующего эндартериита и к тому времени, когда очаг подвергается распаду, кровеносные сосуды, исключая крупные, подвергаются облитерации и кровохарканья нет. Кровохарканье может при этом наступить, если распад образуется очень быстро и если сосуды не облитерированы. Крупные же сосуды не облитерируются, хотя стенка их теряет свою эластичность, благодаря воздействию на них туберкулотоксинов, а перекидываются через каверну как балки и под воздействием тока крови могут расширяться, т. е. образуются аневризмы. При напряжении аневризма может разорваться и дать сильное кровотечение.
Кровохарканье может наступить также при переходе процесса со стенки каверны на стенки сосуда в месте его вхождения в каверну и при разъедании стенки сосуда. Небольшие кровохарканья нередко возникают и при фиброзных процессах, когда кровеносные сосуды, обычно мелкие, значительно деформируются развивающейся соединительной тканью. При их разрыве возникает кровохарканье.
Кровохарканье и особенно кровотечение – это грозное осложнение туберкулезного процесса, требующее немедленных врачебных вмешательств.
Мероприятия по остановке легочного кровотечения должны осуществляться следующим образом:
1. Снижение давления в малом круге кровообращения (назначение противокашлевых средств, разгрузка малого круга кровообращения).
2. Уменьшение проницаемости сосудистой стенки.
3. Повышение свертываемости крови.
Применявшиеся ранее широко искусственный пневмоторакс и пневмоперитонеум при лечении легочных кровотечений в настоящее время используются редко и только в случаях отсутствия эффекта от консервативной терапии и возможности осуществить при трахеобронхоскопии санацию или эндоваскулярную эмболизацию бронхиальных артерий. При этом следует подчеркнуть, что пневмоторакс при хроническом туберкулезе часто оказывается неэффективным из-за плевральных сращений. Чаще используемый в этих целях пневмоперитонеум может оказывать гемостатическое действие главным образом при легочных кровотечениях у больных с нижнедолевым деструктивным туберкулезом легких.
С внедрением и усовершенствованием эндоскопических и эндоваскулярных методов хирургии можно добиться гемостаза практически у всех больных с легочным кровотечением, за исключением молниеносных, когда летальный исход наступает в течение 5 мин, что не позволяет организовать реальную помощь больному. Поэтому в проведении комплекса лечебных мероприятий больному с легочным кровотечением должны принимать участие не только фтизиатр-терапевт, а также анестезиолог, эндоскопист и хирург.
Спонтанный пневмоторакс развивается вследствие нарушения целостности висцеральной плевры с образованием сообщения плевральной полости с воздухоносными путями. Причиной его возникновения может быть не только туберкулез, но и травма грудной клетки, неспецифические заболевания легких, буллезная эмфизема, кисты, опухоли, пневмокониозы и др.
Несмотря на многообразие этиологических факторов, патогенез спонтанного пневмоторакса определяется следующими постоянными компонентами: нарушением герметичности плевральной полости, отслойкой висцеральной плевры от париетальной, сдавлением (коллапсом) легкого, смещением средостения в здоровую сторону. За счет этого могут развиваться: коллапс легкого с возникновением дыхательной недостаточности, раздражение рецепторов париетальной плевры с болевым синдромом вплоть до плеврального шока, возникновение острой сердечно-сосудистой недостаточности.
Различают открытый спонтанный пневмоторакс, при котором сохраняется постоянное сообщение с атмосферным воздухом; клапанный (наиболее тяжелый), когда вследствие действия «клапанного» механизма в плевральной полости увеличивается количество воздуха, повышается положительное давление; закрытый, при котором после проникновения воздуха в плевральную полость сообщение между ней и атмосферным воздухом прекращается.
Клиническая картина и исход каждого из трех видов спонтанного пневмоторакса различны.
Ограниченный закрытый спонтанный пневмоторакс может протекать бессимптомно. Выраженных гемодинамических расстройств у таких больных не бывает. Перфорация висцеральной плевры, как правило, быстро закрывается. Такой пневмоторакс редко осложняется экссудативным плевритом, через некоторое время газовый пузырь рассасывается и легкое расправляется.
Открытый спонтанный пневмоторакс протекает более длительно и тяжелее, чем закрытый, так как при нем очень часто возникает экссудативный плеврит, обусловленный смешанной микробной флорой.
Наиболее тяжелое течение наблюдается при клапанном пневмотораксе. Нарастающее положительное давление в плевральной полости увеличивает одышку и ведет к нарушению деятельности сердца. Состояние больного отягощается присоединением гнойного плеврита.
Диагностика спонтанного пневмоторакса несложна. Кроме клинических симптомов дыхательной недостаточности, у больных отмечаются тимпанический звук при перкуссии, ослабленное дыхание над соответствующей половиной грудной клетки. Наличие газового пузыря и коллапса легкого подтверждается при рентгенологическом исследовании.
Лечение заключается в оказании неотложной помощи при резко выраженной дыхательной недостаточности и нарушении деятельности сердечно-сосудистой системы. Назначают строгий постельный режим, противокашлевые, болеутоляющие и сердечные средства, оксигенотерапию. Применяется также специфическая и неспецифическая общая и местная химиотерапия (профилактика эмпиемы). Дальнейшая тактика лечения определяется для каждого больного индивидуально. Некоторым больным необходимо произвести плевральную пункцию и аспирацию воздуха, если в плевральной полости создается высокое положительное давление. Иногда такие аспирации нужно делать повторно или можно поставить подводный дренаж. Больным с открытым или клапанным пневмотораксом в случае отсутствия эффекта от консервативной терапии нужно выполнить операцию.
Амилоидоз внутренних органов. Амилоидоз внутренних органов является одним из осложнений хронических форм туберкулеза и возникает вследствие нарушения белкового обмена в организме и выражается в выпадении гомогенных белковых масс в межтканевых щелях по ходу сосудов, их стенках и оболочках железистых органов.
Различают распространенный амилоидоз и местное отложение амилоида. При общем амилоидозе наиболее часто поражается селезенка, затем печень, почки, надпочечники, кишечник и другие органы. В результате отложения амилоида нарушается метаболизм в расположенных вблизи клетках; они и другие тканевые элементы сдавливаются, атрофируются. Амилоидоз развивается медленно и неблагоприятно сказывается на течении основного процесса.
При осмотре больных амилоидозом обращает на себя внимание бледность и одутловатость лица, связанная с отечностью подкожной клетчатки, а иногда и с анемией. Поражение почек обычно протекает с нефротическим синдромом. В начальный период болезни поражение почек существенно не отражается на общем состоянии больного. Лишь исследование мочи позволяет выявить протеинурию, причем в отличие от «чистого» нефротического синдрома в моче обнаруживаются не только альбумины, но и глобулины. В осадке мочи определяются не только цилиндры – гиалиновые, зернистые, восковидные, но и лейкоциты, эпителиальные клетки и небольшое количество эритроцитов. Однако у части больных наблюдается выраженный нефротический синдром с типичными для него изменениями мочи.
Исследования крови выявляют гипопротеинемию с характерным сдвигом в сторону преобладания глобулинов (альбумин-глобулиновый коэффициент уменьшается до 1,0 и ниже).
В более поздний период появляются отеки, часто возникает асцит, вначале болезни – полиурия, при прогрессировании – олигурия с высоким удельным весом и большим количеством белка в моче. Артериальная гипертензия, несмотря на поражение почечных сосудов, при амилоидозе наблюдается редко. Нарушение клубочковой фильтрации происходит уже в ранний период болезни. В конечной стадии возникает картина выраженной почечной недостаточности с азотемией и уремией.
На успех в лечении амилоидоза можно рассчитывать только в том случае, если устранена причина болезни и еще нет грубых изменений в органах, прежде всего в почках. Лечение включает диету с повышенным содержанием белка (при достаточной азотвыделительной функции почек) и ограничением хлорида натрия, витаминотерапию, борьбу с отеками и азотемией (при почечной недостаточности).
Легочно–сердечная недостаточность.
Функция аппарата внешнего дыхания направлена на обеспечение организма кислородом и удаление образовавшейся в процессе обменных реакций углекислоты. Многие острые и хронические заболевания бронхов и легких приводят к развитию дыхательной недостаточности, причем степень морфологических изменений в легких далеко не всегда соответствует степени недостаточности их функции.
Дыхательную недостаточность принято определять как состояние организма, при котором не обеспечивается поддержания нормального газового состава крови либо оно достигается за счет более интенсивной работы аппарата внешнего дыхания и повышенной нагрузкой сердца, что приводит к снижению функциональных возможностей организма. Функция аппарата внешнего дыхания очень тесно связана с функцией системы кровообращения, при недостаточности внешнего дыхания усиленная работа сердца является одним из важных элементов ее компенсации.
Различают три основных типа вентиляционных нарушений: рестриктивный, обструктивный и смешанный.
Рестриктивный тип обусловлен уменьшением дыхательной поверхности, выключением легкого или части его из вентиляции, снижением эластической растяжимости легочной паренхимы, ограничением подвижности диафрагмы и т. д.
Обструктивный тип нарушений легочной вентиляции обусловлен сужением просвета дыхательных путей, что ведет к затруднению прохождения воздуха по бронхам.
Смешанный тип объединяет признаки обоих предыдущих типов, часто с превалированием одного из них.
Клинически дыхательная недостаточность проявляется одышкой, цианозом, а в поздней стадии – при присоединении сердечной недостаточности – и отеками.
Включение различных компенсаторных механизмов в борьбе с прогрессирующей дыхательной недостаточностью происходит постепенно, адекватно ее степени. На ранних стадиях дыхательной недостаточности функция аппарата внешнего дыхания в покое осуществляется обычным путем. Лишь при выполнении больным физической работы подключаются компенсаторные механизмы (имеется только снижение резервных возможностей). В дальнейшем и при небольшой нагрузке, а затем даже в покое наблюдаются тахипноэ, тахикардия, определяются признаки усиленной работы дыхательной мускулатуры при вдохе и выдохе, участие в акте дыхания дополнительных групп мышц. В более поздних стадиях дыхательной недостаточности, когда организм исчерпывает компенсаторные возможности, выявляются артериальная гипоксемия и гиперкапния.
В более поздний период к легочной недостаточности присоединяется сердечная (правожелудочковая) недостаточность вследствие развития гипертонии малого круга кровообращения, сопровождающейся повышенной нагрузкой на правый желудочек сердца. Трудно установить, когда именно к легочной недостаточности присоединяются симптомы изменения системы кровообращения, т. к. признаки легочной и сердечной недостаточности очень близки.
Легочное сердце обычно развивается у лиц, длительно страдающих заболеванием легких. У больных старше 50 лет оно возникает быстрее, чем у более молодых, что связано с меньшими компенсаторными возможностями легочной циркуляции и миокарда пожилых.
Диагностика компенсированного легочного сердца без инструментальных методов исследования трудна. Такие симптомы как одышка и цианоз могут быть легочного и сердечного происхождения. В стадии компенсации легочного сердца, когда правый желудочек справляется с повышенными требованиями циркуляции, имеются только легочная гипертензия и гипертрофия правого желудочка. Среди физических признаков повышенного давления в малом круге кровообращения основным является акцент II тона над легочной артерией. Компенсированное легочное сердце должно быть подтверждено с помощью инструментальных методов (рентгенологического, электро- векторкардиографии и др.).
В клинической практике очень важно распознать начальные признаки декомпенсации. Симптомы ее: усталость, анорексия и потеря в массе тела, нарастание одышки (в покое), боли в правом подреберьи. Они свидетельствуют о надвигающейся декомпенсации легочного сердца.
Классификация хронического легочного сердца.
I степень – неспособность системы осуществлять функцию не обнаруживается в покое и проявляется лишь изредка при повышенной нагрузке (невозможность приспособиться к увеличению объема или интенсивности выполняемого труда).
II степень — нарушение функций систем в покое не обнаруживается, но постоянно возникает при выполнении повседневной нагрузки.
III степень – неспособность системы осуществлять функцию обнаруживается не только при нагрузке, но и в покое.
Лечение компенсированного легочного сердца сводится к лечению основного заболевания, которое привело к нарушению вентиляции, предупреждению простуд, отказу от курения (никотин вызывает общую легочную вазоконстрикцию). Декомпенсированное легочное сердце требует комплексного лечения, направленного на устранение респираторной недостаточности (противовоспалительные, бронхолитические, муколитические препараты, лечебная дыхательная гимнастика); артериальной гипоксемии, гиперкапнии и ацидоза (оксигенотерапия, стимуляторы дыхания, коррекция кислотно-щелочного равновесия); спазма легочных артериол (ганглиоблокаторы, спазмолитики, антикоагулянты), а также лечение слабости миокарда (сердечные гликозиды, диуретики, препараты, улучшающие метаболизм миокарда).
- Материалы методического обеспечения занятия.
6.1. Учебно-методическая литература:
– основная:
1. Петренко В.І. Фтизіатрія підручник В.І. Петренко, В.Ф. Москаленко, Ю.І. Фещенко та ін. — В. Нова Книга, 2006. – с. 196-211 (електронна книга).
2. Туберкульоз: Підручник для студ.мед.навч.закл./За ред.-проф.О.К.Асмолова 2002.–с. 198-205.
3. Туберкульоз: Підручник для студ.мед.навч.закл. III-IV рівнів акредитації (електроний ресурс) / О.К.Асмолов. О.А.Бабуріна, І.М.Смольська, Н.А.Герасимова, 2003. – с. 198-205.
4. Петренко В.И. Фтизиатрия учебник. — К. Медицина, 2008. – с. 321-335 (електронна книга).
5. Асмолов О.К., Бабуріна О. А, Герасимова Н. А. Практична підготовка з фтизіатрії, 2010, навчальний посібник. – с. 6-9, 81-84 (електронна книга).
— дополнительная:
1. Фещенко Ю.І. Контроль за туберкульозом в умовах адаптованої ДОТС-стратегії / Ю.І.Фещенко, В.М.Мельник. — К.: Медицина, 2007. – 478 с.
2. Наказ МОЗ України від 16.08.2010 № 684 „Про затвердження Стандарту інфекційного контролю за туберкульозом у лікувально-профілактичних закладах, місцях довгострокового перебування людей та проживання хворих на туберкульоз”
3. Наказ МОЗ України від 21.12.2012 р., № 1091 «Уніфікований клінічний протокол первинної, вторинної (спеціалізованої) та третинної (високоспеціалізованої) медичної допомоги. Туберкульоз».
4. Наказ МОЗ України № 600 „Стандарт надання медичної допомоги хворим на хіміорезистентний туберкульоз” від 22.10.2008.
5. Наказ МОЗ України № 276 „Клінічний протокол надання медичної допомоги хворим на поєднані захворювання – туберкульоз та ВІЛ-інфекцію” від 28.05.2008.
6.2. 0риентирующая карта по самостоятельной работе студента с литературой по теме занятия (выполняется письменно).
Рекомендуемые страницы:
Источник


