Оценка риска кровотечений при фибрилляции предсердий
Шкала HAS-BLED – это простой и надежный клинический инструмент для оценки риска большого кровотечения в течение 1 года. Под большим кровотечением подразумевается: любое интракраниальное кровоизлияние, кровотечение, требующее госпитализации, или сопровождающееся снижением гемоглобина >2 г/л, или требующее гемотрансфузии. Шкала была создана на основе реальной когорты, состоящей из 3978 больных с фибрилляцией предсердий.
Шкала оценки риска кровотечения была представлена Р. Пистером и др. в 2010 г. [1] и была названа HAS-BLED как акроним:
Hypertension — гипертония
Abnormal renal/liver function – нарушение функции почек и печени
Stroke — инсульт
Bleeding history or predisposition – кровотечения в анамнезе и/или предрасположенность к ним
Labile international normalized ratio – лабильное международное нормализованное отношение (МНО)
Elderly – возраст (>65 лет)
Drugs/alcohol concomitantly – совместный прием медикаментов и/или алкоголя
1 балл присваивается за каждый пункт, результат – это простая сумма баллов. Максимальное число баллов по шкале – 9.
Эффективность любого антитромботического лечения должна быть сбалансирована с риском большого кровотечения, особенно внутримозгового, которое часто является фатальным. Поэтому, риск кровотечения должен быть оценен до назначения антикоагулянтов у больных с фибрилляцией предсердий. Больные с высоким риском кровотечения (балл по шкале HAS-BLED >3) должны проходить регулярное клиническое обследование после начала пероральной антикоагулянтной терапии.
Шкала HAS-BLED включена в европейские и канадские рекомендации по лечению фибрилляции предсердий с 2010 года. Шкала была валидирована на различных независимых когортах и хорошо коррелирует с риском внутримозгового кровоизлияния [2, 3]
Гипертония
Неконтролируемая, систолическое АД >160 мм рт.ст.)
Нет
Есть
Нарушение функции почек
Хронический диализ, либо трансплантация почки, либо креатинин сыворотки более 200 мкмоль/л (>2.26 мг/дл)
Нет
Есть
Нарушение функции печени
Хронические болезни печени (цирроз), либо значительные сдвиги в печеночных пробах (повышение билирубина> 2 раза от верхней границы нормы + повышение АЛТ/АСТ/щелочной фосфатазы > 3 раза от верхней границы нормы)
Нет
Есть
Инсульт
В анамнезе, особенно лакунарный
Нет
Есть
Кровотечения
Большие кровотечения в анамнезе (интракраниальное, либо требующее госпитализации, либо со снижением Hb>2 г/л, либо требующее гемотрансфузию), анемия или предрасположенность к кровотечениям
Нет
Есть
Лабильное МНО
<60% времени в терапевтическом диапазоне
Нет
Есть
Возраст
>65 лет
65 лет и младше
Лекарства
Совместный прием лекарств, усиливающих кровоточивость: антиагреганты, НПВП
Нет
Есть
Злоупотребление алкоголем
>8 стаканов в неделю
Нет
Есть
Список литературы:
- Pisters R, Lane DA, Nieuwlaat R, de Vos CB, Crijns HJ, Lip GY.A novel user-friendly score (HAS-BLED) to assess 1-year risk of major bleeding in patients with atrial fibrillation: the Euro Heart Survey.Chest. 2010 Nov;138(5):1093-100.
- Authors/Task Force Members, Camm AJ, Lip GY, De Caterina R, et al. 2012 focused update of the ESC Guidelines for the management of atrial fibrillation: An update of the 2010 ESC Guidelines for the management of atrial fibrillation * Developed with the special contribution of the European Heart Rhythm Association.Eur Heart J. 2012 Nov;33(21):2719-47.
- Lip GY, Frison L, Halperin JL, Lane DA.Comparative validation of a novel risk score for predicting bleeding risk in anticoagulated patients with atrial fibrillation: the HAS-BLED (Hypertension, Abnormal Renal/Liver Function, Stroke, Bleeding History or Predisposition, Labile INR, Elderly, Drugs/Alcohol Concomitantly) score. J Am CollCardiol. 2011 Jan 11;57(2):173-80.
Вконтакте
Одноклассники
Google+
Источник
Шкалы риска тромбоэмболии при фибрилляции предсердий
Лечение подразумевает установление причины аритмии, восстановление синусового ритма или контроль ЧСС при сохранении фибрилляции предсердий (ФП), а также профилактику системных тромбоэмболий.
Лечение пациента с фибрилляцией предсердий (ФП):
Установление причины аритмии
Выбор стратегии — контроль частоты или контроль ритма сердца
Профилактика системных тромбоэмболий
Во время фибрилляции предсердий (ФП) в ушке ЛП может возникать стаз крови, что ведет к образованию тромбов и системным эмболиям. Особое внимание следует обратить на риск развития инсульта. Также возможны тромбоэмболии сосудов конечностей и органов брюшной полости.
Было обнаружено, что при фибрилляции предсердий (ФП) увеличиваются уровни фибриногена и D-димера в плазме крови. Содержание этих веществ нормализуется после кардиоверсии, поэтому предполагается, что ФП сама по себе может вызывать состояние гиперкоагуляции.
Показано, что варфарин (антагонист витамина К), как и новые ингибиторы тромбина (такие как дабигатран) и ингибиторы фактора Ха (такие как апиксабан и ривароксабан), заметно снижает риск эмболии. Аспирин гораздо менее эффективен, чем варфарин (риск инсульта на фоне приема аспирина снижается всего на 19% против 70%). Недавно проведенный анализ поставил под сомнение факт, что аспирин, являющийся столь же частой причиной кровотечения, как и варфарин, способен предотвращать развитие системных тромбоэмболии.
Вероятность системных тромбоэмболии вследствие фибрилляции предсердий (ФП) можно уменьшить при помощи:
Антагонистов витамина К (например, варфарина)
Ингибиторов тромбина (например, дабигатрана)
Ингибиторов фактора Ха (например, апиксабана)
Аспирина (гораздо менее эффективен, чем все вышеперечисленные средства)
Следует заметить, что, хотя ишемический инсульт у пациентов с фибрилляцией предсердий (ФП) в значительной части случаев является следствием эмболии из ЛП, до 25% инсультов у таких пациентов развиваются вследствие цереброваскулярной болезни или наличия атероматозных бляшек в сонных артериях либо в проксимальном отделе аорты.
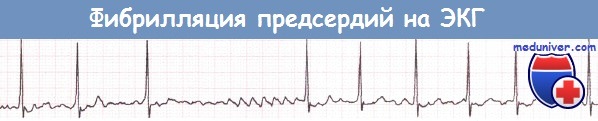
Типичные волны f и абсолютно нерегулярный ритм желудочков при фибрилляции предсердий (ФП).
Риск тромбоэмболии при фибрилляции предсердий
При фибрилляции предсердий (ФП), обусловленной ревматическим поражением митрального клапана, риск инсульта резко увеличивается (в 15 раз). Строго показано назначение варфарина.
При фибрилляции предсердий (ФП) «неревматической» этиологии (главным образом на фоне сердечной недостаточности или артериальной гипертензии) риск инсульта оценивается как умеренно высокий (5-кратное увеличение) с частотой возникновения около 5% в год. Наличие в анамнезе системной эмболии также ассоциировано с высоким риском. С другой стороны, у пациентов с идиопатической формой ФП риск эмболии составляет менее 1 % в год.
На риск системных эмболических осложнений, вероятнее всего, не влияет форма течения ФП — пароксизмальная или персистирующая.
Для оценки риска инсульта при неклапанной ФП были предложены две балльные системы, учитывающие ряд факторов риска.
Шкала CHADS2
С — сердечная недостаточность;
Н — наличие артериальной гипертензии в анамнезе;
А — возраст 75 лет и старше;
D — сахарный диабет;
S — наличие инсульта или транзиторной ишемической атаки в анамнезе. (Используются начальные буквы англоязычных терминов, обозначающих эти состояния.)
Каждому из этих факторов риска присваивается по 1 баллу, за исключением последнего — ему присваиваются 2 балла, поэтому после буквы S стоит цифра 2. Для каждого больного вычисляется набранная сумма баллов.
При помощи полученных сумм баллов 0, 1 и 2-6 оценивают риск инсульта как низкий, средний и высокий соответственно. Вопрос о назначении антикоагулянтов следует рассмотреть при наличии >2 баллов. Если число баллов < 1, рекомендуется использовать аспирин или вообще не назначать антитромботическую терапию.
Тем не менее было показано, что у некоторые пациентов, имеющих < 1 балла по шкале CHADS2, велик риск инсульта. Поэтому для определения риска у пациентов этой категории была создана более сложная балльная система.

Шкала CHA2DS2VASc
Как указано выше, С — сердечная недостаточность; Н — наличие артериальной гипертензии в анамнезе; А — возраст 75 лет и старше; D — сахарный диабет; S — наличие инсульта или транзиторной ишемической атаки в анамнезе.
При наличии каждого из этих факторов риска начисляется по 1 баллу, кроме возраста >75 лет и наличия инсульта или транзиторной ишемической атаки в анамнезе, которым присваиваются по 2 балла.
Дополнительные факторы риска, которые учитываются в данной шкале: V — сосудистые заболевания (ИМ, осложненная бляшка в аорте, заболевание периферических артерий); А — возраст 65-74 года; S — пол (женский). При наличии каждого из этих дополнительных факторов начисляется по 1 баллу.
Если число баллов равно 0, это свидетельствует об очень низком риске и отсутствии необходимости назначения антикоагулянтов. При 1 балле по данной шкале риск расценивается как промежуточный (1,3% в год), в связи с чем рекомендуется рассмотреть вопрос о целесообразности назначения непрямых антикоагулянтов.
Если получено 2 балла и более, то риск инсульта является высоким (2,2% в год при 2 баллах и повышается примерно до 10% в год при сумме баллов более 5), поэтому в таких случаях существует строгое показание для назначения непрямых антикоагулянтов.
— Также рекомендуем «Антикоагулянты для профилактики тромбоэмболии при фибрилляции предсердий»
Оглавление темы «Фибрилляция и трепетание предсердий»:
- ЭКГ при фибрилляции предсердий (ФП)
- Причины фибрилляции предсердий и их прогноз
- Классификация фибрилляции предсердий
- Шкалы риска тромбоэмболии при фибрилляции предсердий
- Антикоагулянты для профилактики тромбоэмболии при фибрилляции предсердий
- Лечение фибрилляции предсердий стратегией контроля частоты
- Лечение фибрилляции предсердий стратегией контроля ритма
- Лечение рефрактерной (стойкой) фибрилляции предсердий
- ЭКГ при трепетании предсердий (ТП)
- Причины трепетания предсердий
Источник
Шкала CHA2DS2-VASc, которая в настоящее время используется для оценки риска инсульта и тромбоэмболий у пациентов с фибрилляцией предсердий (ФП), также может использоваться для этой цели у пациентов с сердечной недостаточностью. К таким выводам пришли авторы датского исследования, которое показало наличие ассоциации между оценкой по CHA2DS2-VASc и риском ишемического инсульта, тромбоэмболий и смерти у пациентов с сердечной недостаточностью как при наличии ФП, так и без этого нарушения ритма. Данные были представлены на проходившем с 29 августа по 2 сентября 2015г. в Лондоне ежегодном конгрессе Европейского общества кардиологов (ESC) и одновременно опубликованы в журнале Journal of the American Medical Association.
Исследователи сообщили, что C-статистика для оценки по шкале CHA2DS2-VASc в отношении предсказания инсульта у пациентов с сердечной недостаточностью, но без фибрилляции предсердий составила 0,64. Обычно значение С-статистики выше 0,70 означает высокое качество прогнозирования, а ниже 0,60 низкое качество, так что полученный результат указывает на промежуточную ценность данного показателя с точки зрения оценки риска инсульта и тромбоэмболий у пациентов с сердечной недостаточностью.
Полученные результаты также могут указывать на целесообразность антикоагулянтной терапии у пациентов с сердечной недостаточностью, но без фибрилляции предсердий при наличии оценки по CHA2DS2-VASc 3 балла (то есть, с двумя дополнительными факторами риска). Также было обнаружено, что у пациентов с сердечной недостаточностью и оценкой по CHA2DS2-VASc 4 балла и более абсолютный риск ишемического инсульта, тромбоэмболий и смерти был очень высоким. Более того, риски тромбоэмболических событий у пациентов с высокими оценками по CHA2DS2-VASc на фоне сердечной недостаточности без ФП оказались выше, чем при фибрилляции предсердий. Это позволяет предположить, что у пациентов с сердечной недостаточностью могут существовать дополнительные механизмы развития инсульта помимо ФП.
Для целей данного исследования были проанализированы три датских национальных регистра – Национальный регистр пациентов (в котором фиксируются все случаи госпитализации и диагнозы); Национальный регистр назначений (который содержит данные обо всех рецептах, по которым были выданы препараты аптеками в Дании) и Регистр системы записи актов гражданского состояния (в котором содержится информация о дате рождения, дате смерти и половой принадлежности всех живущих в Дании людей).
В общей сложности популяция исследования включала 42 987 пациентов в возрасте 50 лет и старше, которые были выписаны с основным диагнозом сердечной недостаточности в период между 2000 и 2012 гг. Из них 21,9% исходно имели диагноз фибрилляции предсердий. Пациенты на антикоагулянтах из анализа исключались.
Как и предполагается шкалой CHA2DS2-VASc, пациентам присваивалось по 1 баллу при наличии застойной сердечной недостаточности, артериальной гипертонии, возраста в диапазоне 65 -74 лет, сахарного диабета, сосудистых заболеваний и женского пола, и по 2 балла, если они были в возрасте 75 лет и старше или перенесли тромбоэмболии ранее. Таким образом, оценку 1 балл могли иметь лишь пациенты с сердечной недостаточностью без каких-либо дополнительных факторов риска.
Риски и ишемического инсульта, и других тромбоэмболий, и смертности увеличивались по мере нарастания оценки по CHA2DS2-VASc независимо от наличия или отсутствия сопутствующей фибрилляции предсердий.
Частота конечных точек (%) через 1 год после диагностирования сердечной недостаточности
Количество факторов риска, входящих в шкалу CHA2DS2-VASc
1
2
3
4
5
6
Пациенты без ФП
Ишемический инсульт
0,4
0,4
0,6
1,0
1,3
2,6
Тромбоэмболические события
1,6
2,0
2,6
3,5
4,5
7,5
Смертность
2,1
2,4
5,7
8,7
9,8
12,9
Пациенты с ФП
Ишемический инсульт
1,5
1,0
1,1
1,7
2,2
3,6
Тромбоэмболические события
3,3
2,9
3,0
3,4
4,7
6,9
Смертность
2,0
4,2
9,5
13,8
15,0
18,9
Тромбоэмболические события = комбинированная конечная точка, в которую входили ишемический инсульт, транзиторная ишемическая атака, системные эмболии, тромбоэмболия легочной артерии и острый инфаркт миокарда
В своей статье авторы обращают внимания, что в общей популяции пациентов с ФП уровень риска инсульта более 1% в год используется в качестве отрезной точки при идентификации тех пациентов, у которых преимущества долгосрочной антикоагуляции перевешивают риски кровотечений. При этом в описанной ими популяции пациентов с сердечной недостаточностью пациенты без ФП и с оценкой по CHA2DS2-VASc 2 балла и выше имели годовой риск инсульта более 1%.
Разумеется, речь идет об обсервационном исследовании, результатов которого недостаточно, чтобы оказать влияние на рутинную практику, и которое должно в будущем послужить основой для рандомизированного исследования. Тем не менее, практикующим врачам уже сейчас имеет смысл иметь в виду тот факт, что риск инсульта существует и при сердечной недостаточности без ФП, и что при увеличении числа входящих в CHA2DS2-VASc факторов у пациента может быть оправданным назначение антикоагулянтов, особенно новых оральных антикоагулянтов.
Источник.
Источник
Материалы для сайта подготовлены сотрудниками лаборатории клинических проблем атеротромбоза Института Кардиологии им. А.Л.Мясникова


(резюме документа, выпущенного European Heart Rhythm Association, и утвержденного рабочей группой Европейского общества кардиологов по тромбозам).
Общая популяция пациентов с мерцательной аритмией
- У большей части пациентов с мерцательной аритмией (МА) частота тромбоэмболических осложнений без антикоагулянтной терапии значительно выше (в 5-8 раз), чем частота кровотечений; поэтому большая часть пациентов с МА (включая большинство пациентов с высоким риском кровотечений) нуждается в терапии антикоагулянтами.
- В лечении пациентов, нуждающихся в постоянной антикоагулянтной терапии, следует руководствоваться рекомендациями ESC по ведению пациентов с мерцательной аритмией.
- Риск кровотечений на фоне приема аспирина сопоставим с риском на фоне приема антагонистов витамина К (АВК), особенно у пожилых пациентов.
- Преимущества от приема АВК имеются у большинства пациентов с высоким индексом CHA2DS2-VASc (таблица 1) даже на фоне высокого риска кровотечения. Только у небольшого количества больных с относительно низким риском инсульта и очень высоким риском кровотечения может быть решено воздержаться от назначения АВК.
- У всех пациентов с МА рекомендовано оценивать (долгосрочный) риск кровотечения.
- В особых подгруппах пациентов с МА (после аблации, после окклюзии ушка левого предсердия, после чрескожного коронарного вмешательства (ЧКВ)/острого коронарного синдрома (ОКС)) оценка риска кровотечения является частью ведения таких пациентов, также как и сопоставление этого риска с риском тромбоэмболических осложнений.
- Для оценки риска кровотечения следует использовать шкалу HAS-BLED (гипертония, нарушенная почечная/печеночная функция, инсульт, кровотечение в анамнезе или предрасположенность к кровотечению, лабильное МНО, пожилой возраст (старше 65 лет), злоупотребление алкоголем (более 8 порций в неделю – прим. переводчика) и/или сопутствующий прием ряда лекарств, усиливающих кровоточивость (прим. переводчика)) (таблица 1). Сумма баллов ≥ 3 соответствует высокому риску кровотечений, поэтому проведение антитромботической терапии требует осторожности и регулярного контроля (как на фоне назначения АВК, так и аспирина).
Таблица 1. Шкалы CHA2DS2-VASc и HAS-BLED для оценки риска инсульта и кровотечения.

* — застойная сердечная недостаточность определяется как систолическая дисфункция ЛЖ умеренной или средней тяжести (ФВ ЛЖ менее 40%).
Пациенты, которым выполняется аблация по поводу МА
- Необходимо начать терапию пероральными антикоагулянтами (например, АВК, таким, как варфарин, с достижением уровня МНО 2-3) как минимум за 4 недели до процедуры аблации.
- Зачастую терапия пероральными антикоагулянтами может быть продолжена во время процедуры аблации.
- Если запланирован «мост» из парентеральных антикоагулянтов, пероральные антикоагулянты следует отменить за 2-5 дней до процедуры и вводить гепарин (нефракционированный или низкомолекулярный) до дня, предшествующего аблации.
- Тактика антикоагуляции во время процедуры аблации: после введения интродьюсера и транссептальной пункции следует внутривенно болюсно ввести гепарин (5000 -10000 Ед или 50-100 Ед/кг) с последующей инфузией гепарина 1000-1500 Ед/час с достижением АВС (активированное время свертывания) 300 сек и выше с проверкой этого показателя каждые 30-45 минут. По окончании процедуры прекратить инфузию гепарина, удалить интродьюсер при достижении субтерапевтического уровня АВС (<160 сек); если АВС остается выше, возможно введение протамина. Через 12-24 часа следует возобновить инфузию гепарина с поддерживающей дозой 1000 Ед/час (без дополнительного болюса), целевой уровень АЧТВ 60-80 сек или вдвое выше исходного уровня. Пероральные антикоагулянты следует возобновить в день процедуры.
- Следует заменить нефракционированный гепарин (НФГ) на низкомолекулярный гепарин (НМГ) после первых 12-24 часов, возобновить пероральные антикоагулянты. Прекратить введение НМГ после достижения МНО 2,0 и более.
- Продолжить прием варфарина минимум в течение 12 недель после аблации. Пациенты с индексом CHA2DS2-VASc ≥ 2 должны принимать пероральные антикоагулянты длительно.
Антикоагулянтная терапия при имплантации кардиостимуляторов и кардиовертеров-дефибрилляторов
- Имплантация устройств на фоне продолжающегося приема пероральных антикоагулянтов так же безопасна, как и на фоне терапии «моста», но значительно сокращает длительность госпитализации.
- В некоторых ситуациях лечение пероральными антикоагулянтами должно быть прервано и заменено на гепарин.
- Если процедура имплантации проводится на фоне антикоагуянтов и/или антиагрегантов, операцию должен проводить опытный хирург, уделяющий большое внимание гемостазу и ревизии ложа корпуса стимулятора.
Пациенты с ОКС и/или с потребностью в проведении ЧКВ
- Тактика антикоагулянтной терапии у таких пациентов описана в рекомендациях ESC по ведению больных с МА, а также в консенсусном документе рабочей группы по тромбозам ESC.
Тактика при геморрагических осложнениях
- Необходимо выполнять комплекс необходимых мероприятий для профилактики кровотечений, как периоперационных, так и в рамках длительного лечения.
- Необходимо регулярно переоценивать риск кровотечений. Модифицируемые факторы риска кровотечений должны быть скорректированы.
По материалам:
Bleeding risk assessment and management in atrial fibrillation patients. Summary of a Position Document from the European Heart Rhythm Association, endorsed by the ESC Working Group on Thrombosis. European Heart Journal 2012: 33; 147–156.
https://eurheartj.oxfordjournals.org/content/33/2/147.full.pdf+html
Источник