Кровотечение при повреждении печени и селезенки
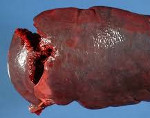
Разрыв селезенки – это нарушение целостности селезенки в результате травматического воздействия. Возникает при ударе в нижнюю часть левой половины грудной клетки или в область левого подреберья. Часто сочетается с повреждением других органов брюшной полости. Проявляется болями в левом подреберье и симптомами кровопотери, обычно наблюдаются признаки раздражения брюшины. Диагноз выставляется на основании клинических проявлений, данных лапароскопии и других исследований. Лечение оперативное — ушивание селезенки или удаление органа.
Общие сведения
Разрыв селезенки – достаточно распространенное повреждение. Из-за высокой вероятности обильного кровотечения представляет непосредственную опасность для жизни, требует проведения немедленного оперативного вмешательства. Чаще встречается у лиц трудоспособного возраста, что обусловлено их более высокой физической активностью и более высоким риском попадания в экстремальные ситуации.
Разрывы селезенки могут быть изолированными, встречаться в составе сочетанной и множественной травмы (политравмы). Часто наблюдаются одновременные повреждения печени, брыжейки и толстой кишки. Возможно сочетание с переломами ребер, повреждением грудной клетки, переломом позвоночника, ЧМТ, переломом таза, переломами костей конечностей и другими повреждениями. Лечение данной патологии осуществляют травматологи и абдоминальные хирурги.

Разрыв селезенки
Причины
Разрыв селезенки встречается при различных высокоэнергетических травмах: падениях с высоты, промышленных, природных, железнодорожных или автодорожных катастрофах. К числу предрасполагающих факторов, повышающих вероятность повреждения селезенки, относятся недостаточно прочная тонкая капсула, полнокровие органа и его малая подвижность. С другой стороны, эти факторы нивелируются тем, что селезенка достаточно надежно защищена от внешних воздействий ребрами. Вероятность разрыва селезенки в результате травмы увеличивается при патологических процессах, сопровождающихся спленомегалией и повышением рыхлости паренхимы. Кроме того, прочность селезенки в некоторой степени зависит от степени ее кровенаполнения, положения органа в момент травмы, фазы дыхания, наполнения кишечника и желудка.
Патанатомия
Селезенка – паренхиматозный орган, расположенный в верхней левой части брюшной полости, кзади от желудка, на уровне IX-XI ребер. Покрыта капсулой. Имеет форму удлиненной и уплощенной полусферы, которая выпуклой стороной обращена к диафрагме, а вогнутой – к органам брюшной полости. Селезенка не относится к числу жизненно важных органов. Является основным источником лимфоцитов, продуцирует антитела, участвует в разрушении старых тромбоцитов и эритроцитов, выполняет функцию депо крови.
Классификация
В абдоминальной хирургии выделяют следующие виды разрывов селезенки:
- Контузия – наблюдается разрыв участка паренхимы при сохранении целостности капсулы органа.
- Разрыв капсулы без значительного повреждения паренхимы.
- Одномоментный разрыв селезенки – одномоментное повреждение капсулы и паренхимы.
- Двухмоментный разрыв селезенки – разрыв паренхимы, за которым через некоторое время следует разрыв капсулы.
- Разрыв капсулы и паренхимы с самостоятельной тампонадой (мнимый двухмоментный разрыв) – разрыв паренхимы быстро «закрывается» сгустком крови и кровотечение прекращается еще до появления выраженной клинической симптоматики. В последующем сгусток вымывается током крови, кровотечение возобновляется.
- Мнимый трехмоментный разрыв – двухмоментный разрыв, за которым через некоторое время следует самостоятельная тампонада, а позже – свободное позднее кровотечение.
Чаще всего наблюдаются одномоментные разрывы селезенки с немедленным возникновением кровотечения в брюшную полость. Двухмоментные разрывы составляют около 13% от общего количества закрытых повреждений селезенки, временной период между моментом травмы и началом кровотечения в брюшную полость колеблется от нескольких часов до 1-2,5 недель. Причиной разрыва капсулы при уже имеющейся центральной или подкапсульной гематоме становится физическое напряжение, чихание, кашель, ходьба, акт дефекации, поворот в постели и другие обстоятельства, вызывающие повышение давления в селезенке.
Большинство разрывов селезенки небольшие, сопровождаются стертой симптоматикой и диагностируются лишь через несколько часов, когда состояние больного ухудшается из-за продолжающейся кровопотери и скопления достаточного количества крови в брюшной полости. Профузное кровотечение с резким нарастанием клинических симптомов чаще наблюдается при двухмоментных повреждениях селезенки.

Возможно, здесь скрыты шокирующие фото медицинских операций
Разрыв селезенки
Симптомы разрыва селезенки
Клиника повреждений селезенки отличается большим разнообразием. Выраженность и наличие тех или иных проявлений зависят от степени разрыва, наличия или отсутствия сопутствующих повреждений, а также времени с момента травмы. Сразу после травматического воздействия может наблюдаться либо нерезкое ухудшение состояния, либо картина острой кровопотери без перитонеальных признаков, свидетельствующих о повреждении паренхиматозного органа. Основными жалобами в первые часы являются боли в районе левого подреберья и верхних отделах живота. Примерно у половины пациентов боли иррадиируют в левую лопатку и левое плечо.
Большинство больных принимают вынужденную позу: на левом боку с поджатыми ногами либо на спине. Брюшная стенка не участвует в акте дыхания. Степень напряжения брюшной стенки и выраженность болевого синдрома при пальпации живота может значительно варьировать как у разных больных, так и у одного и того же пациента в разные периоды после травмы. В отдельных случаях (при коллапсе или шоке) напряжение мышц живота может отсутствовать. Притупление звука в отлогих отделах живота при перкуссии наблюдается только при значительном кровотечении. Через некоторое время после травмы развивается парез кишечника, проявляющийся отсутствием дефекации, задержкой газов и вздутием живота.
Наряду с местными симптомами, наблюдается картина нарастающей острой кровопотери: бледность, липкий холодный пот, снижение АД, учащение пульса, рвота и тошнота, головокружение, прогрессирующая слабость, одышка и шум в ушах. В дальнейшем возможно двигательное возбуждение, сменяющееся потерей сознания, а также учащение пульса свыше 120 уд/мин и снижение АД ниже 70 мм рт. ст. При этом точно установить причину кровотечения на основании одних лишь клинических признаков удается не всегда, поскольку большинство перечисленных выше симптомов (за исключением болей в левом подреберье) непатогномоничны и появляются при любых острых катастрофах в животе.
Диагностика
Анализы крови на начальных этапах обследования малоинформативны, поскольку из-за механизмов компенсации кровопотери состав периферической крови может оставаться в пределах нормы в течение нескольких часов. Диагноз выставляется на основании клинических признаков, данных рентгенографии грудной клетки и рентгенографии живота. На рентгеновских снимках слева под диафрагмой определяется гомогенная тень. Дополнительными признаками разрыва являются ограничение подвижности и высокое стояние левого купола диафрагмы, расширение желудка, смещение левой части ободочной кишки и желудка вправо и книзу. При скудной клинической симптоматике, подкапсульных и центральных гематомах селезенки данные рентгенографии часто неспецифичны. Может потребоваться ангиография, однако этот метод не всегда применим из-за больших временных затрат, отсутствия необходимого оборудования или специалистов.
В настоящее время в связи с широким распространением эндоскопических методов все большее значение в диагностике разрывов селезенки приобретает лапароскопия. Эта методика позволяет не только быстро подтвердить наличие кровотечения в брюшную полость, но и точно установить его источник. При отсутствии эндоскопического оборудования альтернативой лапароскопии может стать лапароцентез – метод, при котором переднюю брюшную стенку прокалывают троакаром (полым инструментом), затем вводят через троакар катетер и выполняют аспирацию содержимого брюшной полости. Данная методика дает возможность подтвердить наличие кровотечения в брюшную полость, но не позволяет установить его источник.
Лечение разрыва селезенки
Кровотечения при подобных повреждениях крайне редко останавливаются самостоятельно, поэтому такая травма является показанием для экстренного хирургического вмешательства. Операция должна быть проведена в как можно более ранние сроки, поскольку нарастающая кровопотеря ухудшает прогноз. При возможности перед началом вмешательства добиваются стабилизации гемодинамики, осуществляя переливание крови и кровезаменителей. Если гемодинамические показатели не удается стабилизировать, операцию проводят даже при тяжелом состоянии пациента, параллельно продолжая осуществлять активные реанимационные мероприятия.
Классическим общепризнанным в травматологии и абдоминальной хирургии способом остановки кровотечения при любых разрывах селезенки считается полное удаление органа. Однако в последние годы, наряду с полным удалением, при отрывах фрагментов и неглубоких одиночных повреждениях некоторые хирурги в качестве варианта рассматривают органосохраняющую операцию – ушивание ран селезенки. Безусловными показаниями к полному удалению органа являются обширные разрывы и размозжения, разрывы в области ворот, обширные рваные и сквозные раны, невозможность надежного ушивания раны и прорезывание швов. В послеоперационном периоде после ушивания или удаления селезенки продолжают внутривенные инфузии крови и кровезаменителей, проводят коррекцию нарушений деятельности различных органов и систем, назначают обезболивающие и антибиотики.
Источник
Травмы паренхиматозных органов диагностируются у 12-50% больных с повреждениями органов брюшной полости, занимая 2-3-е место [1, 5, 11, 17]. Хирургическая тактика при повреждениях печени, селезенки определяется характером травмы и должна быть направлена в первую очередь на обеспечение гемостаза и холестаза [14-16]. Для достижения окончательного гемостаза при ранениях печени и селезенки применяют прошивание, биологические и синтетические пленки, клеевые композиции, методы неконтактного воздействия (лазерная, плазменная, аргоновая и электро-коагуляции) [2-8, 13, 18, 19]. При обширных раневых дефектах печени, селезенки с размозжением ткани выполняют резекции с гемостазом по ходу и с иссечением нежизнеспособных участков паренхимы, по типу первичной хирургической обработки [11, 14]. При отдельных видах травмы печени возможно выполнение оменто- и френогепатопексии. Нередко развиваются некрозы паренхимы печени, селезенки в зоне швов, с развитием нагноений, вторичных кровотечений, желчных свищей, требующих повторных операций [3, 7, 9, 10, 12]. Одной из причин неудач хирургического лечения травм печени и селезенки является отсутствие четких рекомендаций по выбору метода достижения окончательного гемостаза и определения объема вмешательства в зависимости от тяжести повреждения. Совершенствование методов остановки кровотечения при травмах печени и селезенки, а также разработка критериев выбора рациональной тактики при их повреждениях остаются актуальными и по сей день.
Травма печени и селезенки моделировалась в эксперименте на 138 беспородных собаках обоего пола весом от 7 до 20 кг. Смоделировано 268 травм печени и селезенки. Раны наносили с помощью скальпеля, снабженного ограничителем (68): резаные длиной 3 см и более, глубиной не более 2/3 толщины органа (30) и колото-резаные (38). У 38 животных после обеспечения гемостаза первичной раны печени наносили рану селезенке. Тупую травму живота нанесли 26 животным с развитием подкапсульных (20) и внутриорганных (6) гематом. Из них у 13 животных нанесена тупая травма и печени и селезенки. Разрывы печени и селезенки моделировали интраоперационно путем раздавливания паренхимы зажимом по методике Е.С. Владимировой и соавт. [5] у 41 животного; разрывы диафрагмальной и висцеральной поверхностей печени у 20 и селезенки у 21. Размозженные раны доли и сегмента с повреждением интрапаренхиматозных структур смоделированы на 119 животных: селезенки (88) и печени (31) (когда выполняли резекцию органа). Травму ворот селезенки с повреждением ее сосудистой ножки и последующей спленэктомией нанесли 14 животным (см. таблицу).
Все операции выполняли под внутриплевральным тиопенталовым наркозом. Брюшную полость вскрывали верхнесрединным разрезом. Выводили в операционную рану селезенку, печень. При развитии профузного кровотечения накладывали специальное устройство на питающие сосуды соответствующего участка органа (патент РФ на полезную модель РФ №70622) или мягкий эластический жом (патент РФ №2014802) на паренхиму органа, проксимальнее раны или разрыва для обеспечения временного гемостаза. При травмах печени также применили маневр Прингла (пережатие печеночно-двенадцатиперстной связки) или накладывали эластический жгут на паренхиму органа, проксимальнее раны. Раны ушивали хромированным кетгутом (№2-3) или викрилом на атравматичных колющих иглах.
Техника шва при ранах глубиной до 2/3 толщи органа: иглы вкалывали отступя от края раны (а) 1,0 см на расстоянии 1,0-1,5 см между ними, начиная с середины раны (в-в1), с выколом на противоположной стороне под углом 45° (б) к длине раны, направляя иглы кнаружи и в разные стороны. Потом обе иглы переводили поверх раны на первоначальную сторону и строго напротив выкола еще раз на расстоянии 1,0 см от края раны делали вкол под углом 45° к длине раны, направляя иглы к центру раны, выводили их напротив первого вкола. Концы нитей связывали между собой (патент РФ №2346660) (см. рисунок). Рисунок 1. Схема ушивания резаных ран печени и селезенки. а — рана; в-в1 — нити, последовательность проведения.
Рисунок 1. Схема ушивания резаных ран печени и селезенки. а — рана; в-в1 — нити, последовательность проведения. Рисунок 1. Схема ушивания резаных ран печени и селезенки. б — угол, под которым проводится игла; в-в1 — нити, последовательность проведения.
Рисунок 1. Схема ушивания резаных ран печени и селезенки. б — угол, под которым проводится игла; в-в1 — нити, последовательность проведения.
Предварительно шов был использован на изолированных макропрепаратах печени и селезенки с последующим контрастированием внутриорганных структур. Выявлено, что ушивание ран глубиной до 1/3 толщины органа не приводит к выраженному нарушению архитектоники структур (сосудов и желчных протоков), а при ушивании ран глубиной от 1/3 до 2/3 толщины органа могут наблюдаться подобные изменения. Шов предотвращает прорезывание нитей при сближении краев раны и завязывании узлов и обеспечивает гемостаз.
Сквозные ранения органов ушивали следующим образом: проводили прядь сальника через рану на противоположную поверхность органа. Ушивали раны с помощью предложенного или П-образного шва с обеих сторон, захватывая и сальник (рацпредложение №95822).
При тупой травме с развитием подкапсульных гематом паренхиматозных органов малых размеров — диаметром до 3 см (печень — 10, селезенка — 10) и при отсутствии признаков продолжающегося кровотечения проводили миниинвазивное лечение (патент на изобретение РФ №2321427), из-за опасности вторичного разрыва гематом с последующим кровотечением. При гематомах больших размеров и внутриорганных производили атипичную резекцию соответствующего органа. При размозженных ранах, расположенных по краю органа и разрывах, занимающих целую долю или сегмент с повреждением крупных сегментарно-долевых интрапаренхиматозных структур, производили атипичную резекцию соответствующего участка.
При развитии массивной кровопотери наряду с инфузионной терапией осуществляли реинфузию крови. В большинстве наблюдений дренировали брюшную полость. Животные находились под наблюдением до 1 года.
В сроки от 1 нед до 12 мес проводили повторные операции. Макроскопически оценивали состояние селезенки, печени, их цвет, консистенцию. Селезенку удаляли, печень резецировали, проводили гистологическое исследование в сроки 7, 15, 30, 60, 120, 180, 360 сут после операций. Полученные препараты окрашивали гематоксилином и эозином.
При ранах глубиной до 2/3 толщи органа окончательный гемостаз достигнут в 13 наблюдениях из 15 ранений селезенки и в 12 из 15 ранений печени. Гемостаз удалось обеспечить в 16 из 23 и в 11 из 15 наблюдений при сквозных ранениях селезенки и печени соответственно. При продолжающемся кровотечении применяли дополнительные меры гемостаза. Поверхностные разрывы ушивали с захватом дна раны, но с проведением лигатур вне предполагаемой проекции сегментарных сосудов.
При обширных ранах и разрывах после иссечения нежизнеспособных участков паренхимы с целью гемостаза перевязывали (прошивали) сегментарнодолевые артерии и дополнительно накладывали швы с использованием пластических материалов в качестве подкладки у 8 животных с травмой печени и у 10 животных с травмой селезенки. При разрыве диафрагмальной поверхности селезенки в 6 наблюдениях (рацпредложение №05-1303) и печени в 5 наблюдениях на место разрыва укладывали рассасывающуюся гемостатическую марлю и фиксировали орган к брюшине, покрывающей диафрагму. Аналогично этому, при разрыве висцеральной поверхности селезенки у 3 собак на травмы укладывали гемостатическую марлю и фиксировали орган к большой кривизне желудка, проводя швы через его серозно-мышечный слой. У двух животных при разрыве нижнего полюса селезенки использовали метод «наружного сдавления прядью сальника», с фиксированием гемостатической марли с ушиванием.
При разрыве в проекции центральных сегментов печени глубиной около 2/3 толщи органа производили «поэтажное» ушивание с использованием пластических материалов, перевязкой кровоточащих сосудов in situ и у 2 животных применили ушивание с «наружным сдавлением прядью сальника», рассасывающейся гемостатической марлей. При разрыве висцеральной поверхности печени у 3 животных применили ушивание с использованием гемостатической марли, ТахоКомба и у одного животного для достижения окончательного гемостаза пришлось перевязывать долевую артерию печени.
В общей сложности, резекцию селезенки произвели у 88 собак в 3 сериях. В первой серии резецировали верхний полюс и раневую поверхность укрывали сальником (30 собак). Во второй серии — нижний полюс и раневую поверхность укрывали париетальной брюшиной (23 собаки). В третьей серии резецировали 2/3 органа и рану укрывали рассасывающейся гсмостатической марлей (35 собак). Резекцию печени произвели у 31 собаки также в трех сериях. В первой серии выполнили атипичную резекцию после предварительного прошивания паренхимы гемостатическим швом по границе резекции (8 собак). Во второй серии резекция печени произведена после выполнения маневра Прингла (8 собак). В третьей серии резецировали печень (15 животных), и среди них с использованием жома у 8 собак: предварительно прошивали паренхиму органа через прорези жома гемостатическим швом, отсекали удаляемую часть по краю жома и перитонизировали раневую поверхность органа. Резецированную поверхность укрывали сальником (15 наблюдений), париетальной брюшиной (6 наблюдений), рассасывающейся гемостатической марлей (10 наблюдений). Дополнительные швы вынуждены были наложить при резекциях селезенки у 12 животных и у 7 — перевязывали сосуды в плоскости резекции с помощью разработанного устройства (решение о выдаче патента на полезную модель РФ №2008124330/22(029510)). При резекции печени накладывали дополнительные швы и перевязывали сосудисто-протоковые структуры в плоскости резекции у 9 собак. Резекция печени в среднем занимала 15-18 мин, а селезенки 7-10 мин.
Окончательный гемостаз достигнут у 69 (78,4%) животных при резекциях селезенки (25, 18, 26 наблюдений) и 22 (71%) собак при резекциях печени (6, 5, 11 наблюдений) в первой, второй и третьей сериях соответственно.
При повреждении ворот селезенки и сосудистой ножки (14 животных) производили спленэктомию с аутотрансплантацией ткани селезенки в большой сальник (6), предбрюшинную клетчатку (2), забрюшинное пространство (2), в ложе прямых мышц живота (4). Для этого использовали фрагменты паренхимы органа размером 0,3×1,0×2,0 см.
У животных с ушитыми ранами селезенки и печени послеоперационный период характеризовался благоприятным течением. В послеоперационном периоде погибли 14 (10,4%) собак: вследствие невыхода из наркоза — 6 (резекция верхнего полюса селезенки (2), ушивание разрыва селезенки (1), резекция печени (2), ушивание разрыва печени (1)). Спаечная кишечная непроходимость развилась у 3 животных (резекция нижнего полюса селезенки (2), спленэктомия и аутотрансплантация в большой сальник (1)). Послеоперационный перитонит выявлен у 3 собак (резекция 2/3 селезенки (1) резекция печени (1), ушивание разрыва висцеральной поверхности печени (1)). Кишечное кровотечение отмечено у одной собаки, она погибла на 50-й день после резекции 2/3 селезенки. Одно животное погибло после ушивания разрыва диафрагмальной поверхности печени на 25-е сутки от поддиафрагмального абсцесса. Остальные животные перенесли операцию хорошо.
Морфологические данные, полученные в динамике после операции, свидетельствуют о хорошей регенерации в области оперированной раны.
Клинические наблюдения
Предложенный шов применили в клинической практике при ушивании:
— резаных ран печени (3 наблюдения): длиной до 5 см и глубиной до 2/3 толщины паренхимы 3 и 4 сегментов печени (2 наблюдения), длиной 5,5 см диафрагмальной поверхности правой доли печени без повреждения интрапаренхиматозных структур (один больной);
— резаных ран диафрагмальной поверхности селезенки длиной до 5 см и глубиной до 2/3 толщины органа (2 больных);
— сквозных ран 4 и 5-6 сегментов печени (2 больных) и селезенки (1 больной со сквозной раной, 1 больной с колото-резаной раной нижнего полюса селезенки);
— разрывов печени (4 больным): разрывы до 5,0 см левой доли диафрагмальной поверхности печени (2 пациента), до 5 см диафрагмальной поверхности 5-6 сегментов доли печени (2 наблюдения), из них с тампонадой сальником (3 больных) и рассасывающейся гемостатической марлей (1 больной);
— разрыва диафрагмальной поверхности селезенки размерами до 4,0 см выполнили ушивание с фиксацией к париетальной брюшине.
Атипичные резекции печени с наложением П-образных швов выполнили 2 больным (разрыв до 5,5 см, связанный с травмой живота и размозженная рана левой доли печени размером 4,5 см с повреждением сегментарных внутриорганных структур). Резекцию селезенки выполнили 4 больным (травмы селезенки (3 больных) и киста нижнего полюса (1 наблюдение)). Подкапсульные гематомы около 3,0 см при отсутствии признаков продолжающегося кровотечения лечили миниинвазивно: у 3 больных диафрагмальной поверхности печени (3 и 6 сегменты) и у 1 больной висцеральной поверхности 5 сегмента. Подкапсульные гематомы диафрагмальной поверхности селезенки размерами до 3 см при отсутствии признаков продолжающегося кровотечения лечили миниинвазивным методом у 4 больных (гематомы средней части селезенки — 2 и нижнего полюса — 2). Во всех наблюдениях удалось обеспечить надежный гемостаз.
Разнообразие повреждений печени и селезенки при травме живота определяет сложность выбора рациональной хирургической тактики. Многое зависит от данных интраоперационной ревизии поврежденного органа. После достижения временного гемостаза и эвакуации крови из брюшной полости решающее значение мы придаем оценке характера повреждений. Поверхностные разрывы печени, селезенки ушиваем с захватом дна раны, с проведением лигатуры вне предполагаемой проекции сегментарных сосудов и с фиксацией к линии шва пластического материала для предупреждения прорезывания.
При глубоких разрывах, более 2/3 толщины органа, исключали возможное повреждение крупных долевых (сегментарных) сосудов и протоков [5]. Для достижения гемостаза при разрывах печени, селезенки наряду с ушиванием возможна и изолированная перевязка сегментарных артериальных сосудов. При краевых размозженных ранах и разрывах, занимающих долю или сегмент, производили соответствующую резекцию. При глубоких ранах в области ворот или множественных разрывах селезенки выполняли спленэктомию с имплантацией фрагментов селезенки. Обязательным условием является перитонизация резекционной поверхности печени, селезенки и дренирование зоны вмешательства.
Таким образом, проведенные исследования показали эффективность предложенных способов гемостаза, что позволит улучшить результаты органосохраняющих операций на печени, селезенке при повреждениях.
Источник


