Гемофилия количество тромбоцитов время кровотечения
Гемофилия и ее причины. Тромбоцитопения и ее причины
Гемофилия является геморрагическим заболеванием, которое встречается почти исключительно у мужчин. В 85% случаев оно связано с аномалией или дефицитом фактора VIII; данный тип гемофилии называют гемофилией А, или классической гемофилией. Эта болезнь поражает примерно 1 из 10000 мужчин в США. У 15% больных гемофилией склонность к кровотечениям вызывает дефицит фактора IX. Оба эти фактора передаются генетически женской хромосомой. В связи с этим у женщин практически не бывает гемофилии, поскольку, по крайней мере, одна из Х-хромосом имеет соответствующие гены. Если одна из Х-хромосом женщины дефектна, она считается носителем гемофилии и передает болезнь половине ее мужских потомков и состояние носительства половине ее женских потомков.
Кровоточивость при гемофилии может быть выражена в разной степени в зависимости от характера генетической неполноценности. Нарушение свертывания обычно выявляется лишь после травмы, но у некоторых больных травма, необходимая для вызова сильного и длительного кровотечения, может быть столь незначительной, что ее трудно заметить. Например, после удаления зуба кровотечение часто может продолжаться в течение нескольких дней.
Фактор VIII имеет два активных компонента: большой компонент с молекулярной массой в миллионы и малый компонент с молекулярной массой около 230000. Малый компонент является наиболее важным для внутреннего пути свертывания, и именно недостаток этой части фактора VIII вызывает классическую гемофилию. Другая геморрагическая болезнь, называемая болезнью Виллебранда и имеющая некоторые характерные особенности, возникает в связи с потерей крупного компонента.
Когда у человека с классической гемофилией возникает сильное длительное кровотечение, практически единственно эффективным лечением является инъекция очищенного фактора VIII. Стоимость его очень высока, а доступность — ограничена, поскольку этот фактор получают только из человеческой крови и в чрезвычайно малых количествах.
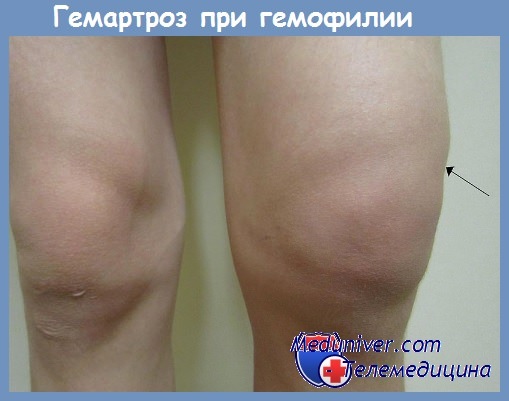
Тромбоцитопения и ее причины
Тромбоцитопения означает очень низкое количество кровяных пластинок в циркулирующей крови. Как и больные гемофилией, люди с тромбоцитопенией склонны к кровоточивости, однако в этом случае кровь обычно течет из многих мелких венул и капилляров, а не из более крупных сосудов, как при гемофилии. В результате во всех тканях тела появляются мелкие точечные кровоизлияния. На коже такого больного видны многочисленные мелкие пурпурные точки, в связи с чем болезнь называют тромбоцитопенической пурпурой. Как указывалось ранее, тромбоциты особенно важны для восстановления мельчайших разрывов капилляров и других мелких сосудов.
Обычно кровоточивости нет до тех пор, пока количество тромбоцитов не упадет ниже 50000/мкл (при норме 150000-300000). Уровни ниже 10000/мкл часто являются летальными.
Даже без специального подсчета тромбоцитов иногда можно предположить наличие тромбоцитопении, если у человека не происходит ретракции сгустка, поскольку, как отмечалось ранее, ретракция в норме зависит от выделения многочисленных факторов коагуляции из большого числа тромбоцитов, захваченных в фибринную сеть тромба.
Люди с тромбоцитопенией в основном имеют так называемую идиопатическую тромбоцитопению, т.е. неизвестного происхождения. В настоящее время известно, что у большинства из этих людей по неизвестным причинам формируются специфические антитела, которые реагируют с тромбоцитами, разрушая их. Для прекращения кровоточивости на 1-4 сут у больных с тромбоцитопенией обычно эффективны переливания свежей цельной крови с высоким содержанием тромбоцитов. Кроме того, часто бывает полезным удаление селезенки (спленэктомия), иногда приводящее к практически полному излечению, поскольку селезенка в норме удаляет большое число тромбоцитов из крови.
— Также рекомендуем «Тромбоэмболические состояния у человека. Причины тромбоэмболий»
Оглавление темы «Свертывающая система. Вентиляция легких»:
1. Внутренний путь инициации свертывания. Роль ионов кальция в свертывании
2. Суммарная инициация свертывания крови. Внутрисосудистые антикоагулянты
3. Лизис кровяных сгустков — плазмин. Повышенная кровоточивость
4. Гемофилия и ее причины. Тромбоцитопения и ее причины
5. Тромбоэмболические состояния у человека. Причины тромбоэмболий
6. Гепарин в виде антикоагулянта. Кумарины
7. Оценка состояния свертывания крови. Протромбиновое время (ПТИ)
8. Легочная вентиляция. Механика легочной вентиляции
9. Движение воздуха в легких. Плевральное и альвеолярное давление
10. Растяжимость легких. Характеристика растяжимости легких
Источник
Гемофилия (кровоточивость) является геморрагическим диатезом, передающимся по наследству, выражающимся в самопроизвольных (спонтанных) или вызванных травмой, иногда очень незначительной, кровотечениях, обусловленных пониженной свертываемостью крови.
Исторические данные. Заболевания гемофилией известны издавна. Ротшильд считал, что первые литературные указания относятся к началу II века нашей эры. Тем не менее первые попытки серьезного изучения и описания болезни произведены лишь в конце XVII столетия.
Фордайс сообщил о кровоточивых семействах и подчеркнул наследственный характер этого заболевания. Шенлейн дал этому геморрагическому диатезу наименование «гемофилия» и подробно его описал.
Грандидье в монографии, основанной на наблюдениях за 200 семействами больных гемофилией, вывел правила наследования этого заболевания. Оказалось, что гемофилией болеют лишь мужчины, но передается заболевание не детям, а внукам через внешне здоровых дочерей.
Сали доказал при гемофилии наличие пониженной свертываемости крови.
Э. Вейль добился хорошего терапевтического эффекта при переливании крови больным гемофилией.
Майнот, Девидсон установили, что плазма крови здорового человека, освобожденная от форменных элементов, сохраняет свой терапевтические свойства, в то время как цельная кровь больного гемофилией, так и плазма его лишены способности нормализовать свертываемость.
Этиология и патогенез. Только что указанные данные, полученные Майнотом и Девидсоном, подводят нас к пониманию патогенеза гемофилии. Кровь больного гемофилией лишена какого-то фактора, имеющегося в нормальной крови. Найдено, что этот фактор связан с глобулинами. Как выше указано, он назван антигемофилический глобулином, тромбопластиногеном.
Таким образом, сущность гемофилии заключается в том, что вследствие недостаточного содержания в плазме антигемофилического глобулина плазмы (фактор VIII) нарушается образование тромбопластина, а это ведет к тому, что очень медленно образуется тромбин. Недостаток антигемофилического глобулина в свою очередь может зависеть от целого ряда отчасти изученных, отчасти малоизвестных факторов. Клиническая картина гемофилии может быть при недостатке фактора IX и плазматической предстадии тромбопластина.
Если выпустить кровь здорового человека, взятую из вены, в пробирку, то она быстро свертывается. Еще до образования сгустка кровяные пластинки исчезают из плазмы. При гемофилии кровь долго не свертывается. Оседают форменные элементы, в первую очередь эритроциты. В плазме взвешены лейкоциты и, что самое важное, тромбоциты.
При пробе по Бюркеру первая ниточка фибрина образуется в нормальной крови через 5 минут. При гемофилии она появляется через 20-50 минут. Сгусток образуется иногда через 2 часа, а иногда и больший срок. Длительность кровотечения (т. е. продолжительность истечения крови из места укола) при гемофилии не отличается от нормальной. Ретракция кровяного сгустка не изменена.
Если к плазме крови страдающего гемофилией прибавить плазму здорового человека, то время свертывания укорачивается.
Возникает вопрос, от какого фактора зависит замедленная свертываемость крови у страдающего гемофилией: от неполноценности кровяных пластинок или от нарушений в составе плазмы — от фактора плазмы.
Количество и морфология тромбоцитов при гемофилии не изменены. Добавление к несвертывающейся плазме больного гемофилией плазмы здорового человека без кровяных пластинок ускоряет свертывание крови: при наличии плазмы здорового человека тромбоциты больного гемофилией выполняют свое назначение. Отсюда ясно, что основными при гемофилии являются нарушения состава плазмы. В плазме недостает, как выше указано, антигемофилического глобулина — тромбопластиногена. Этим объясняется нарушение образования сгустка крови, ее свертывание. Кроме этой классической формы гемофилии (гемофилия А), сейчас описана гемофилия В (болезнь Кристмаса), при которой в крови отсутствует не фактор VIII, а другой (фактор IX, или фактор Кристмаса). Наконец, сейчас описана гемофилия, С, при которой отсутствует фактор X, являющийся предшественником фактора IX. Антигемофилический глобулин имеется у таких больных в достаточном количестве. Гемофилия С встречается и у женщин.
Гемофилией страдают мужчины. Дочери, происшедшие от брака больного гемофилией со здоровой женщиной, передают своему потомству наследственное предрасположение к гемофилии (являются «кондукторами»).
Не описано ни одного достоверного случая страдания женщины гемофилией с полной клинической картиной заболевания, в частности с гемартрозами. Но не так редки случаи, когда дочери отца, страдающего гемофилией, имеют некоторую наклонность к кровопотерям: носовые кровотечения, обильные менструации. Незначительные хирургические вмешательства: экстракция зуба, тонзиллэктомия могут вызвать тяжкие, трудно останавливаемые кровотечения. Больная, наблюдавшаяся Фонио, погибла от обескровливания вслед за незначительным ранением пальца.
У женщин, страдающих подобными явлениями, из семьи больных гемофилией также бывает замедление свертываемости крови.
Интересны данные, полученные при изучении частоты заболевания в семьях больных гемофилией, особенно при условии полноты сведений о всех их членах. Английская королева Виктория была «кондуктором» гемофилии. Из 4 ее сыновей один страдал гемофилией, из 16 внуков — трое, из 20 правнуков — семеро (учащение случаев гемофилии в третьем поколении).
Скелд приводит данные о 60 шведских семействах, где далеко не все мужчины страдают гемофилией. Нередко типичный случай этого заболевания возникает в семье, в которой до того больных гемофилией не было.
Симптомы гемофилии. Кровоточивость проявляется с детства, но при рождении, при перерезке пуповины, особенно сильного кровотечения не наблюдается. В большинстве случаев симптомы гемофилии начинаются в возрасте 2-3 лет. Наблюдаются они при смене молочных зубов. В детском и юношеском возрасте кровотечения особенно опасны. С начала третьего десятилетия жизни они наблюдаются значительно реже.
Незначительный, часто незамеченный больным ушиб может вызвать подкожное, межмышечное или внутрисуставное кровоизлияние. Маленькая рана долго кровоточит.
Наблюдаются кровотечения из желудочно-кишечного тракта (кровавая рвота, кишечное кровотечение), из почек, носовые кровотечения. Встречаются геморрагии и в центральную нервную систему.
Нередки кровоизлияния в полость суставов (коленных, локтевых) — гемартрозы. Они чрезвычайно болезненны. Сустав горяч на ощупь, красен. Околосуставная ткань воспалительно отечна.
Скелд приводит данные о частоте различных кровотечений, наблюдавшихся им у 72 больных: при прорезывании зубов — в 39%, при экстракции зубов — в 37,5% случаев. Кровоизлияния в суставы наблюдались у 90% больных. Наиболее часто они затрагивали коленный (87,5%), локтевой (54%) и голеностопный (53%) суставы.
Кровоизлияние в сустав может рассосаться. Но гораздо чаще излившаяся кровь и выпот организуются. Образуются анкилозы и контрактуры, калечащие больного.
Кениг разделял поражения суставов на три стадии.
1. Кровоизлияние в сустав — гемартроз. В полости сустава жидкая кровь. При соблюдении покоя возможно полное анатомическое и функциональное восстановление сустава.
2. «Панартрит» наблюдается при повторных кровоизлияниях в полость одного и того же сустава. Внешне заболевание похоже на туберкулезное поражение сустава.
3. Контрактура сустава в результате запустевания сустава, резкого изменения синовиальной оболочки и хрящей. Образуются сращения.
Наклонность больных гемофилией к внутримышечным кровоизлияниям заставляет отказываться от введения им лекарственных веществ внутримышечно. Инъекции могут производиться, как правило, подкожно или в вену.
Внутримышечные гематомы обычно хорошо и полностью рассасываются. Однако они могут привести к образованию остеом, фиброзных рубцов с последующим нарушением функции соответствующей мышцы, сдавленней нервов (парезы), сосудов (нарушение питания тканей).
Со стороны внутренних органов при гемофилии не отмечается ничего характерного. Селезенка не увеличена. Исследование крови в период отсутствия обильных кровопотерь показывает нормальное количество эритроцитов, гемоглобина, лейкоцитов, тромбоцитов. Нормальна и лейкоцитарная формула.
Только после кровотечений отмечают появление в крови мелких тромбоцитов и тромбоцитов с нежной зернистостью (юные формы).
Пункция костного мозга при гемофилии не противопоказана. Клеточный состав его не представляется измененным. Разногласия отдельных авторов в этом отношении, видимо, объясняются тем, что одни пунктировали вскоре после обильных кровопотерь, другие — в свободное от кровотечений время. После кровопотерь наблюдается увеличение числа мегакариоцитов, в частности молодых их форм.
Как мы уже указывали, основным симптомом кровоточивости у страдающего гемофилией является замедленная свертываемость крови. Первая ниточка фибрина при пробе по Бюркеру появляется через 20-50 минут (норма 5 минут). Сгусток образуется иногда через 2 часа, иногда и через еще больший срок.
Гемофилия — серьезное заболевание. Оно требует внимательного надзора за мальчиком в период детства и юности. Больному следует избирать профессию, исключающую возможность травм.
Диагноз. Диагноз гемофилии ставится на основании характерных кровотечений, в особенности кровоизлияний в суставы. Болеют мужчины. При исследовании крови характерно нормальное (или даже повышенное) количество тромбоцитов. Характерно замедление свертываемости крови и нормальное время кровотечения. Содержание фибриногена нормальное (в отличие от афибриногенических нарушений свертываемости).
При дифференциальном диагнозе нужно иметь в виду тромбопению (болезнь Верльгофа). При последнем заболевании наблюдается положительный симптом Кончаловского (точечные кровоизлияния на предплечье при наложении жгута на плечо). При гемофилии симптом жгута, как правило, отрицателен. При гемофилии не бывает мелкой, петехиальной сыпи, характерной для тромбопении. Диагноз решает подсчет пластинок.
Наличие поражения суставов может заставить врача при поверхностном исследовании предположить диагноз острого суставного ревматизма. Такой случай (мальчик 8 лет) приводит А. Ф. Тур.
В настоящее время имеются специальные лабораторные методы, позволяющие определить дефицит тромбопластиногена и наличие антигемофилического глобулина в плазме.
Лечение. Гемофилия — неизлечимое заболевание. Все терапевтические мероприятия паллиативны. Лечение должно предприниматься в период кровотечений и кровоизлияний.
Кровоточащая поверхность или рана промывается стерильной горячей жидкостью (раствор соли, новокаин, вода) и плотно тампонируется (лучше — гемостатической губкой, фибринной губкой).
При кровоизлияниях в сустав необходима иммобилизация, применение холода и давящей повязки.
Выделение чистого антигемофилического глобулина для внутривенного введения крайне затруднительно, хотя результаты его применения очень обнадеживающие.
К сожалению, выделенные препараты еще обладают при повторных введениях антигенными свойствами.
В настоящее время основным методом лечения является переливание крови или плазмы. Так как антигемофилический глобулин очень нестоек, то надо производить либо прямое (из вены в вену) переливание крови от донора больному, либо переливание свежей цитратной крови или плазмы (со сроком хранения не более 2-3 часов с момента взятия крови).
Свежая (антигемофилическая) плазма и кровь вливаются в количестве 250-500 мл. Если нужно, переливание повторяется через каждые 6-8 часов до прекращения кровотечения.
Предложено также применение АКТГ (80 ед. в сутки) и кортизона (120-150 мл). Сухая плазма, приготовленная в первые часы после взятия крови, длительно (годами) сохраняет антигемофилический глобулин и также может успешно применяться для лечения больных гемофилией.
По-видимому, в будущем должна будет проводиться диспансеризация больных гемофилией с периодическим введением им антигемофилического глобулина с целью предупреждения развития геморрагических явлений.
Женский журнал www.BlackPantera.ru:
М. Тушинский
Источник
Тромбоциты – это небольшие (2-4 мкм диаметром) дискообразные безъядерные клеточные фрагменты, циркулирующие в кровотоке, чутко реагирующие на повреждения сосуда и играющие критически важную роль в гемостазе и тромбозе. Тромбоциты образуются при фрагментации своих предшественников мегакариоцитов в костном мозге. Из одного мегакариоцита образуется от 5 до 10 тысяч тромбоцитов. Средняя продолжительность жизни тромбоцита составляет 5-9 дней. Старые тромбоциты разрушаются в процессе фагоцитоза в селезёнке и клетками Купфера в печени.
Формы тромбоцитов:
Различают 5 форм тромбоцитов: юные (0 — 0,8 %), зрелые (90,3 — 95,1 %), старые (2,2 — 5,6 %), формы раздражения (0,8 — 2,3%) и дегенеративные формы (0 — 0,2%).
Функции:
Тромбоциты выполняют две основных функции:
- Формирование тромбоцитарного агрегата, первичной пробки, закрывающей место повреждения сосуда;
- Предоставление своей поверхности для ускорения ключевых реакций плазменного свертывания.
Относительно недавно установлено также, что тромбоциты играют важнейшую роль в заживлении и регенерации поврежденных тканей, освобождая из себя в поврежденные ткани факторы роста, которые стимулируют деление и рост поврежденных клеток. Факторы роста представляют собой полипептидные молекулы различного строения и назначения. К важнейшим факторам роста относятся тромбоцитарный фактор роста (PDGF), трансформирующий фактор роста (TGF-β), фактор роста эндотелия сосудов (VEGF), фактор роста эпителия (EGF), фактор роста фибробластов (FGF), инсулиноподобный фактор роста (IGF).
Физиологическая плазменная концентрация тромбоцитов 150 000-300 000 в мкл.
Уменьшение количества тромбоцитов в крови может приводить к кровотечениям. Увеличение же их количества ведет к формированию сгустков крови (тромбоз), которые могут перекрывать кровеносные сосуды и приводить к таким патологическим состояниям, как инсульт, инфаркт миокарда, легочная эмболия или закупоривание кровеносных сосудов в других органах тела.
Неполноценность или болезнь тромбоцитов называется тромбоцитопатия, которая может быть либо уменьшением количества тромбоцитов (тромбоцитопения), либо нарушением функциональной активности тромбоцитов (тромбастения), либо увеличением количества тромбоцитов (тромбоцитоз). Существуют болезни, уменьшающие число тромбоцитов, такие как гепарин-индуцированная тромбоцитопения или тромботическая пурпура, которые обычно вызывают тромбозы вместо кровотечений.
В связи с неточностью описаний, отсутствием фотографической техники и запутанностью терминологии ранних периодов развития микроскопии, время первого наблюдения тромбоцитов точно неизвестно. Чаще всего их открытие приписывается Донне (Париж, 1842), однако есть данные, что их наблюдал еще сам создатель микроскопа, ван Левенгук (Нидерланды, 1677). Термин «кровяные пластинки», который до сих пор является предпочтительным в англоязычной литературе («blood platelets»), был введен Биццоцеро (Турин, 1881), который также сыграл ведущую роль в выявлении связи тромбоцитов с гемостазом и тромбозом. Это впоследствии привело к появлению термина «тромбоцит» (Декхюйзен, 1901), который в русском языке стал основным, а в англоязычной литературе используется исключительно для ядерных клеток-тромбоцитов у не-млекопитающих («thrombocytes»). Кроме того, в русской литературе для тромбоцитов может употребляться термин «бляшка Биццоцеро».
Участие в свертывании:
Особенностью тромбоцита является его способность к активации — быстрому и как правило необратимому переходу в новое состояние. Стимулом активации может служить практически любое возмущение окружающей среды, вплоть до простого механического напряжения. Однако основными физиологическими активаторами тромбоцитов считаются коллаген (главный белок внеклеточного матрикса), тромбин (основной белок плазменной системы свертывания), АДФ (аденозиндифосфат, появляющийся из разрушенных клеток сосуда или секретируемый самими тромбоцитами) и тромбоксан А2 (вторичный активатор, синтезируемый и выбрасываемый тромбоцитами; его дополнительная функция заключается в стимуляции вазоконстрикции).
Активированные тромбоциты становятся способны прикрепляться к месту повреждения (адгезия) и друг к другу (агрегация), формируя пробку, перекрывающую повреждение. Кроме того, они участвуют в плазменном свертывании двумя основными способами — экспонирование прокоагулянтной мембраны и секреция α-гранул.
Экспонирование прокоагулянтной мембраны:
В нормальном состоянии мембрана тромбоцитов не поддерживает реакций свертывания. Отрицательно заряженные фосфолипиды, в первую очередь фосфатидилсерин, сосредоточены на внутреннем слое мембраны, а фосфатидилхолин внешнего слоя связывает факторы свертывания гораздо хуже. Несмотря на то, что некоторые факторы свертывания могут связываться и с неактивированными тромбоцитами, это не приводит к формированию активных ферментативных комплексов. Активация тромбоцита предположительно приводит к активации фермента скрамблазы, который начинает быстро, специфично, двусторонне и АТФ-независимо перебрасывать отрицательно заряженные фосфолипиды из одного слоя в другой. В результате происходит установление термодинамического равновесия, при котором концентрация фосфатидилсерина в обоих слоях выравнивается. Кроме того, при активации имеет место выставление и/или конформационное изменение многих трансмембранных белков внешнего слоя мембраны, и они приобретают способность специфически связывать факторы свертывания, ускоряя реакции с их участием. Активация тромбоцитов имеет несколько степеней, и экспрессия прокоагулянтной поверхности является одной из высших. Только тромбин или коллаген могут вызывать такой сильный ответ. Более слабые активаторы, особенно АДФ, могут вносить вклад в работу сильных активаторов. Однако, они не способны самостоятельно вызвать появление фосфатидилсерина; их эффекты сводятся к изменению формы тромбоцитов, агрегации и частичной секреции.
Секреция α-гранул:
Тромбоциты содержат несколько типов гранул, содержимое которых секретируется в процессе активации. Главными для свертывания являются α-гранулы, содержащие высокомолекулярные белки, такие как фактор V и фибриноген.
Тесты для оценки сосудисто-тромбоцитарного компонента гемостаза:
- Время кровотечения
- Количество тромбоцитов в крови
- Индуцированная агрегация тромбоцитов
Качественные дефекты тромбоцитов, лежащие в основе большого числа геморрагических диатезов, подразделяют на следующие группы:
- Дезагрегационные тромбоцитопатии, обусловленные отсутствием или блокадой мембранных рецепторов тромбоцитов (тромбастения Гланцмана и др.);
- Болезни отсутствия плотных и α-гранул;
- Нарушения высвобождения гранул;
- Нарушения образования циклических простагландинов и тромбоксана А2;
- Дефицит, аномалии и нарушения мультимерности фактора Виллебрандта;
- Нарушения обмена нуклеотидов и транспорта кальция.
Заболевания:
- Ведущие к понижению количества тромбоцитов в крови
- Тромбоцитопения
- Болезнь Верльгофа (идиопатическая тромбоцитопеническая пурпура)
- Тромботическая тромбоцитопеническая пурпура
- Тромбоцитопеническая пурпура, вызванная лекарствами (например, гепарин-индуцированная)
- Болезнь Гоше
- Апластическая анемия
- Ведущие к повышению количества тромбоцитов в крови или к нарушению их функциональности
- HELLP-синдром (Hemolysis, Elevated Liver enzyme values and Low Platelet counts)
- Гемолитический уремический синдром
- Химиотерапия
- Лихорадка Денге
- Тромбоцитоз
- Нарушения способности тромбоцитов к адгезии и агрегации
- Синдром Бернара-Сулье
- Тромбастения Гланцмана
- Синдром Скотта
- Болезнь фон Виллебранда
- Синдром Германского-Пудлака
- Синдром серых тромбоцитов
- Нарушения метаболизма тромбоцитов
- Пониженная циклооксигеназная активность, врожденная или приобретенная
- Дефицит пула тромбоцитов, врожденная или приобретенная
- Заболевания, в которых тромбоциты играют ключевую роль
- Атеросклероз
- Ишемическая болезнь сердца
- Инфаркт миокарда
- Цереброваскулярная болезнь
- Периферическая артериальная окклюзионная болезнь
- Рак
- Малярия
- Астма
- Синдром Самтера
Источник


.jpg)